题目内容
19.某同学组装了如图所示的电化学装置,判断A,B,C,D属于原电池的是A,属于电解池的是BCD:
写出图中各装置的电极反应:
A:阳极Fe-2e-=Fe2+;阴极Ag++e-=Ag溶液的pH升高(填“升高”、“降低”或“不变”).
B:阳极Ag-e-=Ag+;阴极Ag++e-=Ag.
C:阳极4OH--4e-=2H2O+O2↑;阴极Cu2++2e-=Cu.
D:阳极4OH--4e-=2H2O+O2↑;阴极2H++2e-=H2↑.
分析 在所有电极中Fe是最活泼的金属,所以A为原电池,Fe为负极,Fe失电子生成亚铁离子,Ag电极为正极,银离子在正极得电子发生还原反应,BCD为电解池,B为Cu上镀银,CD的阳极为惰性电极,分别为电解硫酸铜溶液和硫酸钠溶液装置,据此分析.
解答 解:在所有电极中Fe是最活泼的金属,所以A为原电池,Fe为负极,Fe失电子生成亚铁离子,Fe-2e-=Fe2+,Ag电极为正极,银离子在正极得电子发生还原反应Ag++e-=Ag,亚铁离子的水解程度小于银离子,所以溶液的pH增大,BCD为电解池,B为Cu上镀银,Ag电极上电极反应式为Ag-e-=Ag+,Cu电极上电极反应式为Ag++e-=Ag,CD的阳极为惰性电极,分别为电解硫酸铜溶液和硫酸钠溶液装置,C中C电极上的电极反应式为4OH--4e-=2H2O+O2↑,Cu电极上电极反应式为Cu2++2e-=Cu,D中阳极上氢氧根离子放电,电极反应式为4OH--4e-=2H2O+O2↑,阴极上氢离子放电生成氢气,电极反应式为2H++2e-=H2↑,
故答案为:A;BCD;
A:阳极Fe-2e-=Fe2+;阴极Ag++e-=Ag;升高;
B:阳极Ag-e-=Ag+;阴极Ag++e-=Ag;
C:阳极4OH--4e-=2H2O+O2↑;阴极Cu2++2e-=Cu;
D:阳极4OH--4e-=2H2O+O2↑;阴极2H++2e-=H2↑.
点评 本题考查了多池串联时,原电池电解池类型的判断以及电极反应式的书写,题目难度不大,注意含有最活泼的金属池子一般为原电池.

练习册系列答案
相关题目
10.粗略测定草木灰中碳酸钾的含量并检验钾元素的存在,需经过称量、溶解、过滤、蒸发、焰色反应等操作.下列图示对应的操作不规范的是( )
| A. |  称量 | B. | 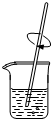 溶解 | C. |  蒸发 | D. | 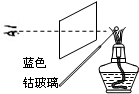 焰色反应 |
14.下列对阿佛加德罗常数NA的说法正确的是( )
| A. | 分子数为0.5NA的氧化钠,其质量为31克 | |
| B. | 标准状况下,4.48升乙烯分子中共含σ键数目为NA | |
| C. | 硫化钾0.5mol/l的溶液中含K+数为NA | |
| D. | 把1mol和0.3molN2与H2混合在一定条件下充分反应生成NH3分子数为0.2NA |
4.下列说法正确的是( )
| A. | 过氧化钠是既有氧化性又有还原性的淡黄色固体 | |
| B. | 铝箔在酒精灯上灼烧可观察到内部熔化但不滴落,说明铝的熔点高 | |
| C. | SiO2属于酸性氧化物,能和水化合生成硅酸 | |
| D. | 二氧化硅可以用来作太阳能电池的材料 |
11.下列化学反应符合“电解质(Ⅰ)+电解质(Ⅱ)═电解质(Ⅲ)+电解质(Ⅳ)”的是( )
| A. | Zn+H2SO4═ZnSO4+H2↑ | B. | CaCO3+2HNO3═Ca(NO3)2+CO2↑+H2O | ||
| C. | CH4+2O2$\stackrel{点燃}{→}$CO2+2H2O | D. | BaCl2+Na2SO4═2NaCl+BaSO4↓ |
8.设NA为阿伏加德罗常数的数值,则下列叙述不正确的是( )
| A. | 1 mol/L MgCl2溶液中含Cl-数为2NA | |
| B. | 标准状况下,2.24 L 18O2中所含中子的数目是2NA | |
| C. | 1 mol Al3+含有核外电子数为10NA | |
| D. | 常温常压下,16 g CH4中含有的原子总数为5NA |
9.下列有关实验的操作、原理和现象,正确的是( )
| A. | 亚硝酸钠不稳定,常温下即会分解,可用作食品添加剂 | |
| B. | 纸层析实验中,滤纸作为惰性支持物,展开剂作为流动相 | |
| C. | 牙膏中的安息香酸钠、氟化钠等溶于水,水解使溶液显酸性 | |
| D. | 欲分离硝酸钾和氯化钠的混合物(物质的量比为1:1),先将样品溶解,然后加热至表面出现晶膜后冷却,过滤得硝酸钾晶体;将母液加热至大量晶体析出后,用余热蒸干,得氯化钠晶体 |
