题目内容
1.有碳酸钠和碳酸氢钠固体混合物3.24g.结合内容回答:(1)除去该混合物中的碳酸氢钠可采取的方法是将混合物加热至不再产生气体为止(加热法).
(2)若将该混合物加热至质量不再变化时,剩余固体质量为2.62g.计算原混合物中碳酸钠的质量分数.
分析 (1)碳酸氢钠加热分解生成碳酸钠;
(2)结合2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑及质量差计算.
解答 解:(1)碳酸氢钠加热分解生成碳酸钠,则除去该混合物中的碳酸氢钠可采取的方法是将混合物加热至不再产生气体为止(加热法),
故答案为:将混合物加热至不再产生气体为止(加热法);
(2)反应前后的质量差为:3.24-2.62=0.62g,
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑△m
2×84g (18+44)g
m(NaHCO3) 0.62g
解得m(NaHCO3)=1.68g,
则碳酸钠的质量为3.24-1.68=1.56g,
碳酸钠的质量分数为$\frac{1.56g}{3.24g}$×100%=48.2%,
答:原混合物中碳酸钠的质量分数为48.2%.
点评 本题考查混合物分离提纯及化学反应的计算,为高频考点,把握物质的性质、发生的反应及差量法计算为解答的关键,侧重分析与计算能力的综合考查,题目难度不大.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案 天天练口算系列答案
天天练口算系列答案
相关题目
18.将下列物质注入水中,振荡后静置,能分层且浮于水面上的是( )
| A. | 溴苯 | B. | 苯 | C. | 乙醇 | D. | 硝基苯 |
19.实验室某试剂瓶上有如下标志: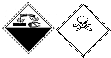 该标志的含义是( )
该标志的含义是( )
 该标志的含义是( )
该标志的含义是( )| A. | 自燃物品、有毒 | B. | 腐蚀品、有毒 | C. | 爆炸性、腐蚀品 | D. | 腐蚀品、氧化剂 |
3.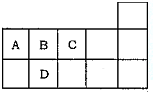 如图为元素周期表短周期的一部分,下列有关A,B,C,D四种元素的叙述正确的是( )
如图为元素周期表短周期的一部分,下列有关A,B,C,D四种元素的叙述正确的是( )
 如图为元素周期表短周期的一部分,下列有关A,B,C,D四种元素的叙述正确的是( )
如图为元素周期表短周期的一部分,下列有关A,B,C,D四种元素的叙述正确的是( )| A. | 原子半径大小比较为D>A>B>C | |
| B. | A与C形成的阴离子可能有AC22-,A2C42- | |
| C. | 生成的氢化物分子间均可形成氢键 | |
| D. | A,B,C,D的单质常温下均不导电 |
6.可以将六种无色液体:C2H5OH、C6H6、AgNO3溶液,NaOH溶液、KI溶液、C6H5OH溶液,区分开的试剂是( )
| A. | 碘水 | B. | 淀粉溶液 | C. | FeCl3溶液 | D. | 新制氢氧化铜 |
13.短周期元素X、Y、Z原子序数依次递增且原子序数和为32,Y、Z在同一周期但不相邻,Z的最外层电子数等于其电子层数.下列有关叙述不正确的是( )
| A. | X、Y两元素能形成阴阳离子个数比都是1:2的化合物Y2X、Y2X2 | |
| B. | Z的简单离子在同周期元素所形成的简单离子中半径最小,Z的最高价氧化物对应的水化物既能与强酸反应又能与强碱反应 | |
| C. | Y、Z所在周期的所有元素中Y的金属性最强,工业上通过电解其熔融氯化物得到Y单质 | |
| D. | X元素形成的单质存在同素异形现象,其中以X2单质最为常见且氧化性最强 |
11.下列物质中能使酸性高锰酸钾溶液褪色的是( )
| A. | 乙烷 | B. | 乙烯 | C. | 乙醇 | D. | 乙酸 |
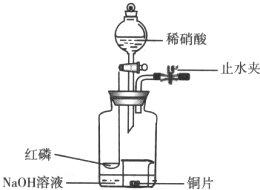 用如图示装置制备NO并验证其还原性.
用如图示装置制备NO并验证其还原性.