题目内容
6.可以将六种无色液体:C2H5OH、C6H6、AgNO3溶液,NaOH溶液、KI溶液、C6H5OH溶液,区分开的试剂是( )| A. | 碘水 | B. | 淀粉溶液 | C. | FeCl3溶液 | D. | 新制氢氧化铜 |
分析 C2H5OH、C6H6、AgNO3溶液、NaOH溶液、KI溶液、C6H5OH溶液分别FeCl3溶液反应的现象分别为:不反应不分层、不反应分层后油状液体在上层,白色沉淀、红褐色沉淀、溶液为浅绿色、溶液为紫色,以此解答.
解答 解:A.碘水不能鉴别C2H5OH、NaOH溶液、KI溶液,故A错误;
B.淀粉与上述溶液均不反应,不能区分,故B错误;
C.C2H5OH、C6H6、AgNO3溶液、NaOH溶液、KI溶液、C6H5OH溶液分别FeCl3溶液反应的现象分别为:不反应不分层、不反应分层后油状液体在上层,白色沉淀、红褐色沉淀、溶液为浅绿色、溶液为紫色,现象不同,能区分,故C正确;
D.均不与氢氧化铜反应,不能区分,故D错误;
故选C.
点评 本题考查物质的区分,为高频考点,注意利用反应的不同现象来区分是解答的关键,侧重物质性质的考查,明确常见有机物、无机物之间的反应即可解答,题目难度中等.

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案
相关题目
3. W、M、X、Y、Z五种短周期元素在周期表中的位置如表所示,其中只有M为金属元素.请回答下列问题:
W、M、X、Y、Z五种短周期元素在周期表中的位置如表所示,其中只有M为金属元素.请回答下列问题:
(1)M的原子结构示意图为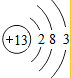 ,比较Y与Z两种元素的简单离子的半径大小:S2->Cl-(用离子符号表示)
,比较Y与Z两种元素的简单离子的半径大小:S2->Cl-(用离子符号表示)
(2)写出X的氧化物与W的氢化物的水溶液反应的化学方程式:SiO2+4HF=SiF4↑+2H2O.
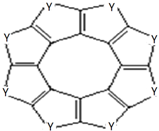
(3)科学家研制出一种英文名为sulflower的新型分子C16Y8(结构如图所示).1mol C16Y8最多能与8mol H2发生加成反应.
(4)托帕石是一种名贵黄玉,其组成为M2[XO4]WOH,托帕在强碱溶液中会发生腐蚀,写出托帕石粉末与过量NaOH溶液反应的化学方程式:Al2[SiO4]FOH+5NaOH=2NaAlO2+Na2SiO3+NaF+3H2O.
 W、M、X、Y、Z五种短周期元素在周期表中的位置如表所示,其中只有M为金属元素.请回答下列问题:
W、M、X、Y、Z五种短周期元素在周期表中的位置如表所示,其中只有M为金属元素.请回答下列问题:| W | ||||
| M | X | Y | Z |
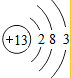 ,比较Y与Z两种元素的简单离子的半径大小:S2->Cl-(用离子符号表示)
,比较Y与Z两种元素的简单离子的半径大小:S2->Cl-(用离子符号表示)(2)写出X的氧化物与W的氢化物的水溶液反应的化学方程式:SiO2+4HF=SiF4↑+2H2O.
(3)科学家研制出一种英文名为sulflower的新型分子C16Y8(结构如图所示).1mol C16Y8最多能与8mol H2发生加成反应.
(4)托帕石是一种名贵黄玉,其组成为M2[XO4]WOH,托帕在强碱溶液中会发生腐蚀,写出托帕石粉末与过量NaOH溶液反应的化学方程式:Al2[SiO4]FOH+5NaOH=2NaAlO2+Na2SiO3+NaF+3H2O.
4.下列物质既能与强酸又能与强碱反应的是( )
①Al(OH)3 ②Al2O3 ③(NH4)2CO3 ④SiO2.
①Al(OH)3 ②Al2O3 ③(NH4)2CO3 ④SiO2.
| A. | ①②③ | B. | ②③④ | C. | ①②④ | D. | ①②③④ |
11.绿色农药--信息素的推广使用,对环保有重要意义.有一种信息素的结构简式为CH3(CH2)5CH=CH(CH2)9CHO.下列检验该信息素中的官能团所用试剂及顺序正确的是( )
| A. | 先加入足量酸性高锰酸钾溶液;后加银氨溶液,水浴加热 | |
| B. | 先加入足量溴水;后加酸性高锰酸钾溶液 | |
| C. | 先加入足量银氨溶液,水浴加热;再另取该物质加入溴水 | |
| D. | 先加入足量新制氢氧化铜悬浊液,加热;再加入溴水 |
18.是常见四种有机物的比例模型示意图,下列说法正确的是( )


| A. | 甲在空气中燃烧时发出明亮的火焰,并伴有黑烟 | |
| B. | SO2使溴水褪色与乙使KMnO4溶液褪色的原理相同 | |
| C. | 丙中的碳碳键的夹角为109°28′ | |
| D. | 丁在稀硫酸作用下可与乙酸发生取代反应并断裂碳氧键 |
15.某同学在实验报告中有以下实验数据,其中数据合理的( )
①用托盘天平称取11.7g食盐
②用量筒量取5.26mL盐酸
③用广泛pH试纸测得溶液的pH是3.5
④用25mL酸式滴定管量出15.80mL的KMnO4溶液.
①用托盘天平称取11.7g食盐
②用量筒量取5.26mL盐酸
③用广泛pH试纸测得溶液的pH是3.5
④用25mL酸式滴定管量出15.80mL的KMnO4溶液.
| A. | ②③ | B. | ①③ | C. | ①④ | D. | 只有① |
16.铝合金是制造飞机、汽车等的常用材料.下列关子${\;}_{13}^{27}$Al的叙述正确的是( )
| A. | 质子数是27 | B. | 中子数是27 | C. | 电子数是13 | D. | 质量数是13 |