题目内容
11.下列物质中能使酸性高锰酸钾溶液褪色的是( )| A. | 乙烷 | B. | 乙烯 | C. | 乙醇 | D. | 乙酸 |
分析 高锰酸钾具有强的氧化性,遇到还原性物质发生氧化还原反应退色,据此解答.
解答 解:A.乙烷性质稳定,与酸性高锰酸钾不反应,不能被酸性KMnO4溶液氧化而褪色,故A错误;
B.乙烯含有碳碳双键,具有强的还原性,能够还原高锰酸钾使其褪色,故B正确;
C.乙醇含有-OH,具有醇的性质,且与羟基相连的碳原子上有氢原子,能被酸性KMnO4溶液氧化而使酸性高锰酸钾褪色,故C正确;
D.乙酸与高锰酸钾不反应,所以乙酸不能被酸性KMnO4溶液氧化而褪色,故D错误;
故选:BC.
点评 本题考查常见有机物物质的结构与性质,熟悉乙烯、乙醇的结构及性质即可解答,题目难度不大.

练习册系列答案
相关题目
2.下列有关一些有机化合物的说法中不正确的是( )
| A. | 乙烯的产量是一个国家石油化工水平的重要标志,工业上主要来源于石油的裂解 | |
| B. | 甲醇也称木醇,无色易挥发液体,有毒.含有甲醇的工业酒精不可饮用 | |
| C. | 甲醛通常条件下是一种无色、有刺激性气味的液体,工业上可用于制取酚醛树脂等 | |
| D. | 苯酚又称石炭酸,无色晶体,有毒,可以用作杀菌消毒剂 |
19.下列不能用勒沙特列原理解释的是( )
| A. | Fe(SCN)3溶液中加入固体KSCN后颜色变深 | |
| B. | 棕红色NO2加压后颜色先变深后变浅 | |
| C. | SO2催化氧化成SO3的反应,往往需要加入过量的氧气 | |
| D. | H2、I2、HI平衡混合气加压后颜色变深 |
6.下列各组中的金属,还原性依次减弱的是( )
| A. | Na,Al,Fe | B. | Zn,Cu,Al | C. | Ca,Na,K | D. | Zn、Ca,Al |
16.铝合金是制造飞机、汽车等的常用材料.下列关子${\;}_{13}^{27}$Al的叙述正确的是( )
| A. | 质子数是27 | B. | 中子数是27 | C. | 电子数是13 | D. | 质量数是13 |
3. 已知X、Y和Z为第三周期元素,其原子的第一至第四电离能如下表:
已知X、Y和Z为第三周期元素,其原子的第一至第四电离能如下表:
(1)X、Y、Z的电负性从大到小的顺序为Al、Mg、Na(用元素符号表示),元素Y的第一电离能大于Z的原因是因为元素Mg价电子排布式为3s2完全充满状态,比Al稳定.
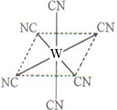
(2)W元素应用广泛,是一种重要的生物金属元素,如人体内W元素的含量偏低,则会影响O2在体内的正常运输.已知W2+与KCN溶液反应得W(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成配合物,其配离子结构如图所示.
①W元素基态原子价电子排布式为3d64s2.
②已知CN-与N2分子互为等电子体,1molCN-中π键数目为2NA.
③上述沉淀溶解过程的化学方程式为Fe(CN)2+4KCN=K4[Fe(CN)6].
 已知X、Y和Z为第三周期元素,其原子的第一至第四电离能如下表:
已知X、Y和Z为第三周期元素,其原子的第一至第四电离能如下表:| 电离能/kJ•mol-1 | I1 | I2 | I3 | I4 |
| X | 496 | 4562 | 6912 | 9543 |
| Y | 738 | 1451 | 7733 | 10540 |
| Z | 578 | 1817 | 2745 | 11578 |
(2)W元素应用广泛,是一种重要的生物金属元素,如人体内W元素的含量偏低,则会影响O2在体内的正常运输.已知W2+与KCN溶液反应得W(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成配合物,其配离子结构如图所示.
①W元素基态原子价电子排布式为3d64s2.
②已知CN-与N2分子互为等电子体,1molCN-中π键数目为2NA.
③上述沉淀溶解过程的化学方程式为Fe(CN)2+4KCN=K4[Fe(CN)6].
20.下列叙述正确的是( )
| A. | 推广使用太阳能、风能、海洋能、氢能,有利于缓解温室效应 | |
| B. | 乙醇和汽油都是可再生能源,应大力推广“乙醇汽油” | |
| C. | 废电池需回收,主要是要利用电池外壳的金属材料 | |
| D. | 升高温度可降低活化能,增大反应速率 |
1.某温度下,在0.1mol•L-1的NaHB强电解质溶液中,c(H+)>c(OH-),则下列关系式一定正确的是( )
| A. | .c(Na+)=c(HB-)+2c(B2-)+c(OH-) | B. | .c(Na+)=0.1mol•L-1≥c(B2-) | ||
| C. | .c(H+)•c(OH-)=10-14 | D. | 此溶液的pH=1 |