题目内容
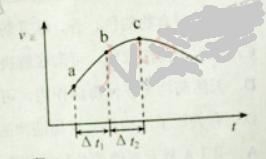
【题目】一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,下列说法正确的是( )

A. a、b、c三点溶液的pH:c<a<b
B. 用湿润的pH试纸测量a处溶液的pH,测量结果偏小
C. a、b、c三点CH3COOH的电离程度:c<a<b
D. a、b、c三点溶液用1 mol·L-1NaOH溶液中和,消耗NaOH溶液体积:c<a<b
【答案】B
【解析】
A.导电能力越强,离子浓度越大,氢离子浓度越大,pH越小;
B.a处溶液稀释时,溶液酸性增强;
C.随水的增多,醋酸的电离程度增大;
D.a、b、c三点溶液浓度不同,但溶质的物质的量相同。
A.导电能力越强,离子浓度越大,氢离子浓度越大,pH越小,则a、b、c三点溶液的pH为b<a<c,A错误;
B.用湿润的pH试纸测量酸性的pH,a处溶液稀释,导电能力增大,溶液酸性增强,pH减小,所以测量结果偏小,B正确;
C.随水的增多,醋酸的电离程度增大,所以a、b、c三点醋酸的电离程度:a<b<c,C错误;
D.a、b、c三点溶液浓度不同,但溶质的物质的量相同,所以a、b、c三点溶液用1mol/L氢氧化钠溶液中和,消耗氢氧化钠溶液体积:a=b=c,D错误;
答案选B。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目