题目内容
【题目】一定条件下,CH4与H2O(g)发生反应:CH4(g)+H2O(g)![]() CO(g)+3H2(g)。设起始
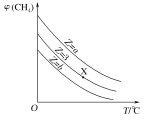
CO(g)+3H2(g)。设起始![]() =Z,在恒压下,平衡时CH4的体积分数φ(CH4)与Z和T(温度)的关系如图所示。下列说法正确的是
=Z,在恒压下,平衡时CH4的体积分数φ(CH4)与Z和T(温度)的关系如图所示。下列说法正确的是
A.该反应的焓变ΔH<0
B.图中Z的大小为a<3<b
C.图中X点对应的平衡混合物中![]() =3
=3
D.温度不变时,图中X点对应的平衡在加压后φ(CH4)减小
【答案】B
【解析】
由图象可知升高温度,甲烷的体积分数减小,说明升高温度平衡正向移动,则正反应为吸热反应,起始![]() =Z,Z越小,说明加入甲烷的物质的量相对水来说越多,含量越大,以此解答该题。
=Z,Z越小,说明加入甲烷的物质的量相对水来说越多,含量越大,以此解答该题。
A. 升高温度,甲烷的体积分数减小,说明升高温度平衡正向移动,则该反应的焓变△H>0,故A错误;
B. 起始![]() =Z,Z越小,说明甲烷相对越多,达到平衡时甲烷的含量越多,则Z的大小为b>3>a,故B正确;
=Z,Z越小,说明甲烷相对越多,达到平衡时甲烷的含量越多,则Z的大小为b>3>a,故B正确;
C. 起始![]() =3,水和甲烷按1:1反应,达到平衡时,二者比值不等于3,故C错误;
=3,水和甲烷按1:1反应,达到平衡时,二者比值不等于3,故C错误;
D. 增大压强,平衡逆向移动,所以平衡在加压后φ(CH4)增大,故D错误。
故答案选:B。

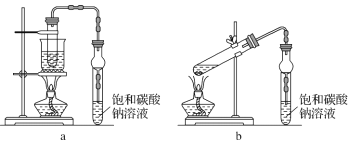
【题目】已知某种燃料含有碳、氢、氧三种元素。为了测定这种燃料中碳和氢两种元素的质量比,可将气态燃料放入足量的O2中燃烧,并使产生的气体全部通过如图所示装置中,得到如表中所列的实验结果(假设产生的气体完全被吸收)。
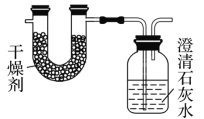
实验前 | 实验后 | |
(干燥剂+U形管)的质量 | 101.1 g | 102.9 g |
(石灰水+广口瓶)的质量 | 312.0 g | 314.2 g |
根据实验数据完成下列问题:
(1)实验完毕后,生成物中水的质量为________g。假设广口瓶里生成一种正盐,其质量为________g。
(2)生成的二氧化碳中碳元素的质量为________g。
(3)该燃料中碳元素与氢元素的质量比为________。
(4)已知这种燃料的每个分子中含有一个氧原子,则该燃料的分子式为________,结构简式为________________。