题目内容
对于反应3Cl2+6NaOH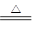 5NaCl+NaClO3+3H2O,以下叙述正确的是
5NaCl+NaClO3+3H2O,以下叙述正确的是
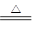 5NaCl+NaClO3+3H2O,以下叙述正确的是
5NaCl+NaClO3+3H2O,以下叙述正确的是| A.Cl2是氧化剂,NaOH是还原剂 |
| B.当有6.72L Cl2反应时,转移电子物质的量为0.5mol |
| C.氧化剂得电子总数与还原剂失电子总数之比为1∶1 |
| D.被氧化的氯原子和被还原的氯原子的物质的量之比为5∶1 |
C
试题分析:A项在该反应属于岐化反应,Cl2既是氧化剂,又是还原剂,错误;B项由于没有告诉气体的标准状况下,无法计算,错误;D项被氧化的氯原子和被还原的氯原子的物质的量之比应该为1∶5,错误。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目


