题目内容
【题目】向一定体积 CaCl2 和 HCl 的混合溶液中逐滴加入浓度为 1.00mol·L-1的 Na2CO3溶液,反应过程中加入的 Na2CO3 溶液的体积与产生沉淀或气体的质量关系如图所示。
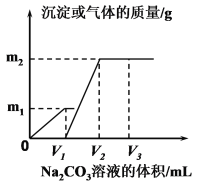
已知:图中 V1 :V2=1:2,当加入 V2mL Na2CO3溶液时,所得溶液的浓度为 1.00 mol·L-1,体积为 200mL。求:
(1)混合溶液中 CaCl2和 HCl 物质的量之比n(CaCl2)∶n(HCl)=_______(2)m2=______g。
【答案】1:25.00
【解析】
试题由图像可知,向一定体积 CaCl2 和 HCl 的混合溶液中逐滴加入浓度为 1.00mol·L-1 的 Na2CO3溶液,0~V1发生的是碳酸钠与盐酸反应,生成二氧化碳的质量为m1,V1~V2发生的是碳酸钠与氯化钙的反应,生成碳酸钙的质量为m2。又知V1:V2=1:2,说明盐酸和氯化钙消耗的Na2CO3 溶液体积相等,由两个反应的化学方程式可知,n(CaCl2)∶n(HCl)= 1:2;当加入 V2mLNa2CO3 溶液时,所得溶液为氯化钠溶液,其浓度为 1.00 mol·L-1,体积为 200mL,所以n(NaCl)=0.200mol,由氯离子守恒可以求出n(CaCl2)=0.0500mol、n(HCl)=0.100mol。
(1)混合溶液中 CaCl2和 HCl 物质的量之比n(CaCl2)∶n(HCl)= 1:2。
(2)由钙离子守恒可知,n(CaCO3)=n(CaCl2)=0.0500mol,所以m2=0.0500mol![]() 5.00g。
5.00g。

 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案【题目】在2 L密闭容器内,800 ℃时NO(g)和O2(g)反应生成NO2(g)的体系中,n(NO)随时间的变化如下表所示:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)上述反应________(填“是”或“不是”)可逆反应,在第5 s时,NO的转化率为________。
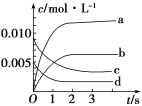
(2)如图,表示NO2变化曲线的是____,用O2表示从0~2 s内该反应的平均速率v=________。
(3)能使该反应的反应速率增大的是________。
a.及时分离出NO2气体
b.适当升高温度
c.增大O2的浓度
d.选择高效的催化剂