题目内容
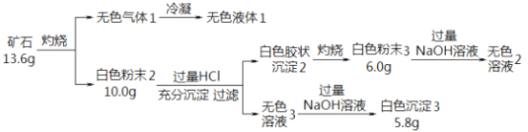
【题目】设计如下实验探究某矿石(仅含四种短周期元素)的组成和性质,已知矿石含有一定的结晶水:
(1)矿石的组成元素是 H、O 和_____、 ______(填元素符号),化学式为_____________。
(2)白色粉末3 溶于NaOH溶液的离子方程式是________。
【答案】Mg,SiMgSiO3·2H2O2OH-+SiO2=SiO32-+H2O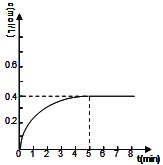
【解析】
根据流程图,矿石灼烧后生成无色气体1,冷凝后得到无色液体1,该无色液体为水,质量为3.6g,物质的量为0.2mol;白色粉末2能够溶于过量盐酸,得到白色胶状沉淀2,和无色溶液3;根据盐酸提供的氢离子和氯离子分析,白色胶状沉淀2可能是氯化银沉淀或硅酸沉淀;白色胶状沉淀2灼烧得到白色粉末3,该物质能够溶于氢氧化钠溶液,说明白色粉末为二氧化硅,不可能为氯化银,因此白色胶状沉淀2为硅酸;无色溶液3中加入过量氢氧化钠得到白色沉淀,说明白色沉淀3为氢氧化镁,5.8g氢氧化镁的物质的量为0.1mol,因此白色粉末2中含有4g氧化镁和6g二氧化硅,因此白色粉末2为硅酸镁。
(1)根据上述分析,矿石的组成元素是 H、O、Mg和Si,硅酸镁的质量为10g,物质的量为![]() =0.1mol,水的物质的量为
=0.1mol,水的物质的量为![]() =0.2mol,因此化学式为MgSiO3·2H2O,故答案为:Mg;Si;MgSiO3·2H2O;
=0.2mol,因此化学式为MgSiO3·2H2O,故答案为:Mg;Si;MgSiO3·2H2O;
(2)白色粉末3为二氧化硅, 溶于NaOH溶液的离子方程式为2OH-+SiO2=SiO32-+H2O,故答案为:2OH-+SiO2=SiO32-+H2O。

【题目】研究弱电解质的电离,有重要的实际意义。
Ⅰ. 醋酸是一种常见的有机酸。
(1)醋酸的电离方程式为__________________________________________________。
(2)保持温度不变,向醋酸溶液中通入一定量的氨气,下列量将变小的是________。
A. c(CH3COO-) B. c(H+)
C. c(OH-) D. CH3COOH电离平衡常数
(3)向0.1 mol·L-1 CH3COOH溶液中加水稀释,c(CH3COO-) / c(CH3COOH)的比值将________(填“变大”、“不变”或“变小”)。
(4)下列事实一定能说明CH3COOH是弱电解质的是____________(填字母)。
A. 相同温度下,浓度均为1 mol·L-1的盐酸和醋酸的导电性对比:盐酸>醋酸
B. 1 mol·L-1 CH3COOH溶液能使紫色石蕊试液变红
C. 25℃时,1 mol·L-1 CH3COOH溶液的pH约为2
D. 10 mL 1mol·L-1的CH3COOH溶液恰好与10 mL 1mol·L-1 NaOH溶液完全反应
Ⅱ. 对比酸性的相对强弱
(5)现有a. CH3COOH b. HCl两种溶液,请回答下列问题(填“>”、“<”或“=”)。
① 将pH相同的两种酸溶液分别稀释100倍后,pH的大小关系为a_______b。
② pH相同、体积相同的两种酸溶液中分别加入足量锌,相同状况下产生气体体积大小关系为a_______b。
③ 将体积相同、pH=2的醋酸和pH=2的盐酸分别与pH=12的氢氧化钠溶液等体积混合,反应后溶液的pH的大小关系为a_______b。
④ 相同物质的量浓度的两种酸溶液中,水的电离程度的大小关系为a_______b。
(6)某些弱酸的电离常数如下:
化学式 | CH3COOH | HSCN | HCN | HClO | H2CO3 |
电 离 常 数 | 1.8×10-5 | 1.3×10-1 | 4.9×10-10 | 3.0×10-8 | K1=4.4×10-7 K2=4.7×10-11 |
①下列反应可以发生的是__________(填字母)。
A. CH3COOH+Na2CO3=NaHCO3+CH3COONa
B. CH3COOH+NaCN=CH3COONa+HCN
C. CO2+H2O+2NaClO=Na2CO3+2HClO
D. NaHCO3+HCN=NaCN+H2O+CO2↑
②25℃时,将20 mL 1 mol·L-1 CH3COOH溶液和20 mL 1 mol·L-1 HSCN溶液分别与20 mL1 mol·L-1 NaHCO3溶液混合,画出产生的CO2气体体积(V)随时间(t)的变化关系图,并注明对应酸的化学式。__________
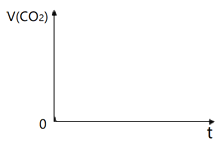 。
。