题目内容
【题目】根据氨气还原氧化铜的反应,可设计测定铜元素相对原子质量Ar(Cu) (近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量m(H2O),由此计算Ar(Cu)。为此,提供的实验仪器及试剂如下(根据需要可重复选用,加入的NH4C1与Ca(OH)2的量足以产生使CuO完全还原的氨气):
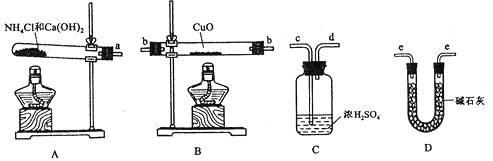
请回答下列问题:
(1)氨气还原炽热氧化铜的化学方程式为________________________________;
(2)从所提供的仪器及试剂中选择并组装本实验的一套合理、简单的装置,按气流方向的连接顺序为(用图中标注的导管口符号表示)a→______________________________;
(3)在本实验中,若测得m(CuO)=ag,m(H2O)=bg,则Ar(Cu)= _______________;
(4)在本实验中,使测定结果Ar(Cu)偏大的是_______________ (填序号);
①CuO未完全起反应 ② CuO不干燥
③CuO中混有不反应的杂质 ④碱石灰不干燥
⑤NH4C1与Ca(OH)2混合物不干燥
(5)在本实验中,还可通过测定_______________和_______________,或_______________和_______________达到实验目的。
【答案】2NH3+ 3CuO![]() 3Cu + 3H2O + N2 a→ e→ b→ e
3Cu + 3H2O + N2 a→ e→ b→ e ![]() -16 ①③ m(CuO) m(Cu) m(Cu) m(H2O)
-16 ①③ m(CuO) m(Cu) m(Cu) m(H2O)
【解析】
(1)氨气具有弱还原性,在加热条件下可以被氧化铜氧化,生成物为氮气、铜和水,反应的化学方程式为2NH3+3CuO![]() 3Cu+3H2O+N2;
3Cu+3H2O+N2;
(2)因为需要测定反应后生成物水的质量,所以必需保证通入的氨气是纯净干燥的,由于浓硫酸可以与氨气反应,因此只能通过碱石灰进行干燥,再通入氧化铜进行反应,最后再通入碱石灰吸收反应生成的水,以测得生成水的质量,所以正确的顺序为a→e→b→e;
(3)根据反应方程式2NH3+3CuO![]() 3Cu+3H2O+N2可知,氧化铜和水的物质的量相等,所以有以下关系式:
3Cu+3H2O+N2可知,氧化铜和水的物质的量相等,所以有以下关系式:![]() =
=![]() ,解得Ar(Cu)=
,解得Ar(Cu)=![]() -16;
-16;
(4)由(3)可知得Ar(Cu)=![]() -16,①若CuO未完全起反应,说明b偏小,结果偏大;②若CuO不干燥,说明a偏小,b偏大,结果偏低;③若CuO中混有不反应的杂质,说明b偏小,结果偏大;④若碱石灰不干燥,说明氨气干燥不彻底,b偏大,结果偏低;⑤若NH4C1与Ca(OH)2混合物不干燥,但只要氨气干燥彻底,对结果不影响;故答案为①③;
-16,①若CuO未完全起反应,说明b偏小,结果偏大;②若CuO不干燥,说明a偏小,b偏大,结果偏低;③若CuO中混有不反应的杂质,说明b偏小,结果偏大;④若碱石灰不干燥,说明氨气干燥不彻底,b偏大,结果偏低;⑤若NH4C1与Ca(OH)2混合物不干燥,但只要氨气干燥彻底,对结果不影响;故答案为①③;
(5)根据反应方程式2NH3+3CuO![]() 3Cu+3H2O+N2可知,也可以通过测定m(CuO)和m(Cu)或m(Cu)和m(H2O)来达到实验目的,故答案为m(CuO)和m(Cu)或m(Cu)和m(H2O)。
3Cu+3H2O+N2可知,也可以通过测定m(CuO)和m(Cu)或m(Cu)和m(H2O)来达到实验目的,故答案为m(CuO)和m(Cu)或m(Cu)和m(H2O)。

 阅读快车系列答案
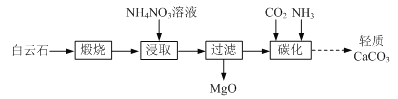
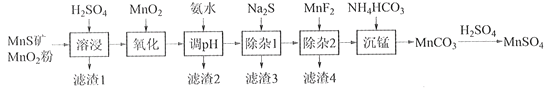
阅读快车系列答案【题目】高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题:
相关金属离子[c0(Mn+)=0.1 mol·L1]形成氢氧化物沉淀的pH范围如下:
金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(1)“滤渣1”含有S和__________________________;写出“溶浸”中二氧化锰与硫化锰反应的化学方程式____________________________________________________。
(2)“氧化”中添加适量的MnO2的作用是将________________________。
(3)“调pH”除铁和铝,溶液的pH范围应调节为_______~6之间。
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是______________。
(5)“除杂2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是_____________________________________________________________________。
(6)写出“沉锰”的离子方程式___________________________________________________。
(7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNixCoyMnz2,其中Ni、Co、Mn的化合价分别为+2、+3、+4。当x=y=![]() 时,z=___________。
时,z=___________。
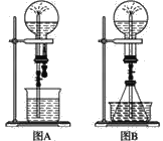
【题目】如图所示,利用培养皿探究NH3的性质。实验时向NaOH固体上滴几滴浓氨水,立即用另一表面皿扣在上面。下表中对实验现象所做的解释正确的是( )

选项 | 实验现象 | 解释 |
A | 浓盐酸附近产生白烟 | NH3与浓盐酸反应产生了NH4Cl固体 |
B | 浓硫酸附近无明显现象 | NH3与浓硫酸不发生反应 |
C | 氯化物溶液变浑浊 | 该溶液一定是AlCl3溶液 |
D | 干燥红石蕊试纸不变色,湿润红石蕊试纸变蓝 | NH3是一种可溶性碱 |
A.AB.BC.CD.D
【题目】(1)室温下,2g苯(C6H6)完全燃烧生成液态水和CO2,放出83.6kJ的热量,写出1molC6H6完全燃烧的热化学方程式:______。
(2)已知:Fe2O3(s)+![]() C(s)=
C(s)=![]() CO2(g)+2Fe(s)△H=+akJmol-1;C(s)+O2(g)=CO2(g)△H=-bkJmol-1,则2Fe(s)+
CO2(g)+2Fe(s)△H=+akJmol-1;C(s)+O2(g)=CO2(g)△H=-bkJmol-1,则2Fe(s)+![]() O2(g)=Fe2O3(s)的△H=________。
O2(g)=Fe2O3(s)的△H=________。
(3)已知几种化学键的键能如表所示:
化学键 | Cl—Cl | F—F | Cl—F |
键能/ kJ·mol—1 | 242 | 159 | 172 |
则反应Cl2(g)+3F2(g)![]() 2ClF3(g)的△H=_____________ kJ·mol-1。
2ClF3(g)的△H=_____________ kJ·mol-1。
(4)如图是乙烷、二甲醚燃烧过程中的能量变化图。
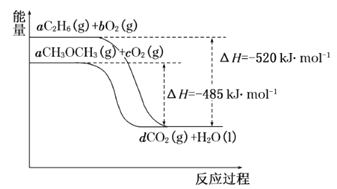
请回答下列问题:
①乙烷的燃烧热ΔH=_______kJ·mol-1。
②根据题图写出二甲醚完全燃烧时的热化学方程式__________。