题目内容
【题目】实验室中有一未知浓度的醋酸,某学生用0.1000 mol·L-1 NaOH标准溶液进行测定醋酸的浓度的实验,取20.00mL待测醋酸放入锥形瓶中,并滴加2~3滴指示剂,用NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。完成下列填空:
实验编号 | 待测醋酸的体积/mL | NaOH溶液的浓度/mol·L-1 | 消耗NaOH溶液的体积/mL |
1 | 20.00 | 0.1000 | 25.18 |
2 | 20.00 | 0.1000 | 23.06 |
3 | 20.00 | 0.1000 | 22.98 |
(1)该实验中指示剂最好选用___________,滴定达到终点的标志是_____________________。
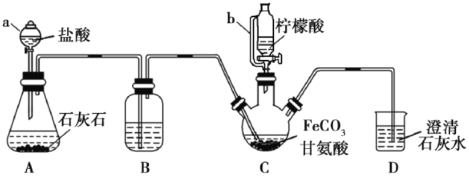
(2)排除碱式滴定管尖嘴中气泡的方法应采用以下_________操作(填甲/乙/丙),然后轻轻挤压玻璃球使尖嘴部分充满碱液。

(3)根据上述数据,可计算出该醋酸的浓度为_________mol·L-1(保留小数点后4位)。
(4)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有________。
A.用滴定管取20.00mL待测醋酸,使用前,水洗后未用待测醋酸润洗
B.锥形瓶水洗后未干燥
C.称量NaOH固体时,有小部分NaOH潮解
D.滴定终点读数时俯视
E.碱式滴定管尖嘴部分有气泡,滴定后消关
【答案】酚酞 加入最后一滴NaOH溶液时,溶液由无色为浅红色且30s内颜色不发生变化 丙 0.115 CE
【解析】
(1)醋酸与氢氧化钠完全反应生成醋酸钠,溶液呈碱性;
(2)由于指示剂酚酞在酸溶液中,所以开始溶液为无色,随加入氢氧化钠增多,pH升高,溶液变为红色;
(2)把碱式滴定管盛满溶液,倾斜45°,再把尖端部分向上倾斜45°,慢慢挤压玻璃珠,使溶液流出,就能赶出气泡;
(3)先计算消耗氢氧化钠溶液的平均体积,再根据 计算醋酸浓度;
计算醋酸浓度;
(4)根据 分析误差。
分析误差。
(1)醋酸与氢氧化钠完全反应生成醋酸钠,溶液呈碱性,选择在碱性范围内变色的指示剂,所以选用酚酞作指示剂;由于指示剂酚酞在酸溶液中,所以开始溶液为无色,当滴加最后一滴NaOH溶液时,溶液由无色恰好变成浅红色且半分钟内不褪色,达到滴定终点。
(2)把碱式滴定管盛满溶液,倾斜45°,再把尖端部分向上倾斜45°,慢慢挤压玻璃珠,使溶液流出,就能赶出气泡,故选丙;
(3)实验1的误差偏离正常范围,根据实验2、3,平均消耗氢氧化钠溶液的体积是![]() mL ,
mL ,  =
=![]() 0.115 mol·L-1 ;
0.115 mol·L-1 ;
(4)A.用滴定管取20.00mL待测醋酸,使用前,水洗后未用待测醋酸润洗,则醋酸浓度偏低,消耗氢氧化钠的体积偏小,测定结果偏低,故不选A;
B.锥形瓶水洗后未干燥,对醋酸物质的量无影响,消耗氢氧化钠的体积不变,测定结果不变,故不选B;
C.称量NaOH固体时,有小部分NaOH潮解,氢氧化钠的浓度偏小,消耗氢氧化钠的体积偏大,测定结果偏高,故选C;
D.滴定终点读数时俯视,消耗氢氧化钠的体积偏小,测定结果偏低,故不选D;
E.碱式滴定管尖嘴部分有气泡,滴定后消关,消耗氢氧化钠体积偏大,测定结果偏高,故选E。

 备战中考寒假系列答案
备战中考寒假系列答案【题目】合理利用资源成为当今研究热点。CH3NH2、PbI2及HI常用作合成太阳能电池的敏化剂甲胺铅碘(CH3NH3PbI3)的主要原料。
(1)制取甲胺的反应为CH3OH(g)+NH3(g)![]() CH3NH2(g)+H2O(g) ΔH。已知该反应中相关化学键的键能数据如下:
CH3NH2(g)+H2O(g) ΔH。已知该反应中相关化学键的键能数据如下:
共价键 | C-O | H-O | N-H | C-N |
键能/kJ·mol-1 | E1 | E2 | E3 | E4 |
则上述热化学方程式中ΔH=___kJ·mol-1。
(2)可利用水煤气合成上述反应所需甲醇。反应为CO(g)+2H2(g)![]() CH3OH(g)ΔH<0。在一定条件下,将1molCO和2molH2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图所示:
CH3OH(g)ΔH<0。在一定条件下,将1molCO和2molH2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图所示:

①平衡时,M点CH3OH的体积分数为10%,则CO的转化率为___。
②图中Y轴表示温度,其判断的理由是__。
(3)可利用四氧化三铅和氢碘酸反应制备难溶PbI2,若反应中生成amolPbI2,则转移电子的物质的量为___。
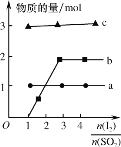
(4)将二氧化硫通入碘水制备HI的反应曲线如图所示,其反应原理为:SO2+I2+2H2O=3H++HSO4-+2I-,I2+I-![]() I3-,图中曲线a、b分别代表的微粒是__和__(填微粒符号);由图知要提高碘的还原率,除控制温度外,还可以采取的措施是___。
I3-,图中曲线a、b分别代表的微粒是__和__(填微粒符号);由图知要提高碘的还原率,除控制温度外,还可以采取的措施是___。