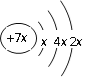题目内容
【题目】下列图示中,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色反应均为黄色。

填写下列空白:
(1)写出化学式:A______________,D______________。
(2)以上反应中属于氧化还原反应的有______________(填序号)。
(3)反应③的化学方程式中:氧化剂是________还原剂是_________
(4)写出反应②的化学方程式:并用双线桥法标出电子转移方向和数目________
【答案】Na Na2CO3 ①②③④ Na2O2 Na2O2 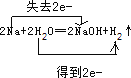
【解析】
B、C、D、E是含A元素的常见化合物,焰色反应为黄色,则A为钠;反应①A与氧气点燃条件产生B,则B为过氧化钠;反应②A与水反应产生C,则C为氢氧化钠;C与过量的二氧化碳反应产生E,则E为碳酸氢钠;E受热易分解,加热产生D,则D为碳酸钠。
根据以上分析可知,A为钠,B为过氧化钠,C为氢氧化钠,D为碳酸钠,E为碳酸氢钠。
(1)化学式:A Na, D Na2CO3;
(2)反应① 2Na+O2![]() Na2O2;
Na2O2;
反应② 2Na+2H2O=2NaOH + H2↑;
反应③ 2Na2O2+2H2O=4NaOH + O2↑;
反应④ 2Na2O2+2CO2=2Na2CO3+ O2;
反应⑤ NaOH+CO2=NaHCO3;
反应⑥ 2NaHCO3![]() Na2CO3+H2O+CO2↑;
Na2CO3+H2O+CO2↑;
综上所述,属于氧化还原反应的有①②③④;
(3)反应③的化学方程式为2Na2O2+2H2O=4NaOH + O2↑,氧化剂和还原剂均是Na2O2 ;
(4) 反应②:2Na+2H2O=2NaOH + H2↑,钠元素化合价升高,氢元素化合价降低,故双键桥为: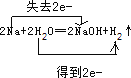 。
。

 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案【题目】下表是元素周期表的一部分,请回答有关问题:
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ | ⑩ |
(1)表中化学性质最不活泼的元素,其原子结构示意图为 _________________________ 。
(2)表中能形成两性氢氧化物的元素是 __________ (用元素符号表示),写出该元素与⑨最高价氧化物的水化物反应的化学方程式 ________________________________ 。
(3)④元素与⑦元素形成化合物的电子式 _________________________ 。
(4)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是 ___________(填化学式)。
(5)③元素与⑩元素两者核电荷数之差是 ____________ 。
(6)设计实验方案:比较⑦与⑩单质氧化性的强弱,请将方案填入下表。
实验步骤 | 实验现象与结论 |
______________ | ________________ |