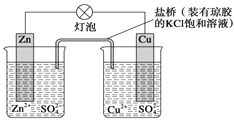
题目内容
【题目】已知几种离子的还原能力强弱顺序为I->Fe2+>Br-,现有200 mL混合溶液中含FeI2、FeBr2各0.10 mol,向其中逐滴滴入氯水(假定Cl2分子只与溶质离子反应,不考虑其他反应)
(1)若氯水中有0.15 mol Cl2被还原,则所得溶液中含有的阴离子主要是________,剩余Fe2+的物质的量为________。
(2)若原溶液中Br-有一半被氧化,共消耗Cl2的物质的量为________,若最终所得溶液为400 mL,其中主要阳离子及其物质的量浓度为________。
(3)通过对上述反应的分析,试判断Cl2,I2,Fe3+,Br2四种氧化剂的氧化能力由强到弱的顺序是_________________________________________________。
(4)上述反应若原溶液中溶质离子全部被氧化后,再滴入足量氯水,则I2全部被Cl2氧化成HIO3(强酸)。试写出此反应的离子方程式:_________________;上述所有反应共消耗Cl2________mol。
【答案】 Cl-、Br- 0.10 mol 0.25 mol n(Fe3+)=0.50 mol/L Cl2>Br2>Fe3+>I2 I2+5Cl2+6H2O===2IO![]() +10Cl-+12H+ 0.8
+10Cl-+12H+ 0.8
【解析】试题分析:(1)根据还原剂的还原性顺序可知,发生的反应依次为2I-+Cl2=I2+2Cl-、2Fe2++Cl2=2Fe3++2Cl-、2Br-+Cl2=Br2+2Cl-,若氯水中有0.15 mol Cl2被还原,则被氧化的是0.2mol碘离子和0.1mol亚铁离子,因此所得溶液中含有的阴离子主要是Br-、Cl-,剩余Fe2+的物质的量为0.2mol—0.1mol=0.1mol。
(2)若原溶液中Br-有一半被氧化,则溶液中的碘离子和亚铁离子已全部被氧化,则根据电子得失守恒可知共消耗Cl2的物质的量为![]() ;若最终所得溶液为400mL,其中铁离子的物质的量浓度为0.2mol÷0.4L=0.5mol/L。
;若最终所得溶液为400mL,其中铁离子的物质的量浓度为0.2mol÷0.4L=0.5mol/L。
(3)根据在氧化还原反应中氧化剂的氧化性强于氧化产物可知Cl2、I2、Fe3+、Br2四种氧化剂的氧化能力由强到弱的顺序是Cl2>Br2>Fe3+>I2。
(4)I2全部被Cl2氧化成HIO3(强酸),则此反应的离子方程式为I2+5Cl2+6H2O=12H++10Cl-+2IO3-。上述所有反应共消耗Cl2的物质的量为![]() 。
。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案