题目内容
【题目】将0.8 mol I2(g)和1.2 mol H2(g)置于某1L密闭容器中,在一定温度下发生反应:I2(g)+H2(g) ![]() 2HI(g) ΔH <0并达到平衡。HI的体积分数随时间的变化如表格所示:
2HI(g) ΔH <0并达到平衡。HI的体积分数随时间的变化如表格所示:
HI体积分数 | 1min | 2min | 3min | 4min | 5min | 6min | 7min |
条件I | 26% | 42% | 52% | 57% | 60% | 60% | 60% |
条件II | 20% | 33% | 43% | 52% | 57% | 65% | 65% |
下列说法中正确的是
A. 在条件I下,该反应的平衡常数K=10
B. 在条件I下,从开始反应至5min,用H2表示的反应速率为0.10 mol/(L·min)
C. 在条件II下,到达平衡时, I2(g)的转化率为81.25%
D. 与条件I相比,为达到条件II的数据,可能改变的条件是降低压强
【答案】C
【解析】A、设I2的消耗浓度为xmol/L,则:
I2(g)+H2(g) ![]() 2HI(g)
2HI(g)
起始浓度(mol/L)0.8 1.2 0
转化浓度(mol/L)x x 2x
平衡浓度(mol/L)0.8-x 1.2-x 2x
平衡时HI的体积分数为60%,则:2x÷2=0.6,故x=0.6,平衡常数K=![]() ,A错误;B、在条件I从开始反应至5min时,H2的反应速率为0.6mol/L÷5min=0.12 mol/(Lmin),B错误;C、在条件II下设I2的消耗浓度为ymol/L,根据A中分析,到达平衡时,2y÷2=0.65,故x=0.65,所以I2(g)的转化率为0.65/0.8×100%=81.25%,C正确;D、相同时间内HI的体积分数减小,说明反应速率减慢,平衡时HI体积分数大于条件I时,故改变条件平衡正向移动,由于压强、催化剂不影响平衡移动,可能是降低温度,D错误,答案选C。
,A错误;B、在条件I从开始反应至5min时,H2的反应速率为0.6mol/L÷5min=0.12 mol/(Lmin),B错误;C、在条件II下设I2的消耗浓度为ymol/L,根据A中分析,到达平衡时,2y÷2=0.65,故x=0.65,所以I2(g)的转化率为0.65/0.8×100%=81.25%,C正确;D、相同时间内HI的体积分数减小,说明反应速率减慢,平衡时HI体积分数大于条件I时,故改变条件平衡正向移动,由于压强、催化剂不影响平衡移动,可能是降低温度,D错误,答案选C。

【题目】[2016·新课标I]锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态Ge原子的核外电子排布式为[Ar]_______________,有__________个未成对电子。
(2)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键。从原子结构角度分析,原因是______________________________。
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因______________________________。
GeCl4 | GeBr4 | GeI4 | |
熔点/℃ | 49.5 | 26 | 146 |
沸点/℃ | 83.1 | 186 | 约400 |
(4)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是______________________________。
(5)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为_______________,微粒之间存在的作用力是_______________。
(6)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置。如图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(![]() ,0,
,0,![]() );C为(
);C为(![]() ,
,![]() ,0)。则D原子的坐标参数为_______________。
,0)。则D原子的坐标参数为_______________。
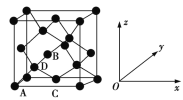
②晶胞参数,描述晶胞的大小和形状。已知Ge单晶的晶胞参数a=565.76 pm,其密度为_____g·cm3(列出计算式即可)。
【题目】下列实验能达到目的的是( )
选项 | 目的 | 实验 |
A | 检验某品牌食盐是否为加碘盐 | 将样品溶解后滴加淀粉溶液 |
B | 检验补铁剂硫酸亚铁片是否部分氧化 | 取样品溶解于水,滴加铁氰化钾溶液 |
C | 鉴别葡萄糖溶液和蔗糖溶液 | 分别取样,滴加银氨溶液,水浴加热 |
D | 证明 | 将 |
A. AB. BC. CD. D
