题目内容
燃烧1 g乙炔生成二氧化碳和液态水,放出热量50 kJ,则这一反应的热化学反应方程式为
- A.2C2H2(g)+5O2(g)====4CO2(g)+2H2O(l);ΔH="+50" kJ·mol-1
- B.C2H2(g)+5/2O2(g)====2CO2(g)+H2O;ΔH="-1" 300 kJ
- C.2C2H2+5O2====4CO2+2H2O;ΔH="-2" 600 kJ
- D.2C2H2(g)+5O2(g)====4CO2(g)+2H2O(l);ΔH="-2" 600 kJ·mol-1
D
本题考查了热化学方程式的书写及简单计算。热化学方程式前面的化学计量数表示物质的量。反应热单位是kJ·mol-1,B和C均错。2 mol C2H2燃烧放出的热量为-2×26×50 kJ·mol-1="-2" 600 kJ·mol-1。
本题考查了热化学方程式的书写及简单计算。热化学方程式前面的化学计量数表示物质的量。反应热单位是kJ·mol-1,B和C均错。2 mol C2H2燃烧放出的热量为-2×26×50 kJ·mol-1="-2" 600 kJ·mol-1。

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
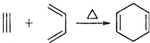 ,如果要合成
,如果要合成 所用的原始原料可以是
所用的原始原料可以是


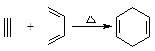 ,如果要合成
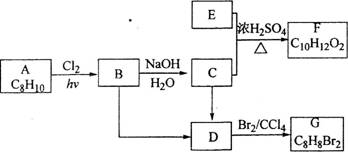
,如果要合成 (1)已知:6.0 g化合物E完全燃烧生成8.8 g CO2和3.6 g H2O;E的蒸气与氢气的相对密度为30,则E的分子式为 ▲ 。
(1)已知:6.0 g化合物E完全燃烧生成8.8 g CO2和3.6 g H2O;E的蒸气与氢气的相对密度为30,则E的分子式为 ▲ 。 ,如果要合成
,如果要合成 所用的原始原料可以是
所用的原始原料可以是