题目内容
已知 0.4 mol 液态肼和足量H2O2反应生成氮气和水蒸气时放出256.64 kJ的热量。
(1)写出肼和H2O2反应的热化学方程式: 。
(2)已知H2O(l)=H2O(g) ΔH="+44" kJ/mol,则16 g液态肼与足量双氧水反应生成氮气和液态水时,放出的热量是 。
(3)上述反应应用于火箭推进器,除释放出大量热量和快速产生大量气体外,还有一个很突出的优点是 。
(4)向次氯酸钠溶液中通入一定物质的量的氨气可生成肼,写出反应的离子方程式: ,该反应的还原产物是 。
(1)N2H4(l)+2H2O2(l) N2(g)+4H2O(g)
N2(g)+4H2O(g)
ΔH="-641.6" kJ/mol
(2)408.8 kJ
(3)产物为氮气和水,对环境无污染
(4)2NH3+ClO- N2H4+Cl-+H2O NaCl
N2H4+Cl-+H2O NaCl
解析

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
化合物A、B是中学常见的物质,其阴阳离子可从下表中选择
| 阳离子 | K+、Na+、Fe2+、Ba2+、NH4+ |
| 阴离子 | OH-、NO3—、I-、HCO3—、AlO2—、HSO4— |
(1)若A、B的水溶液均为无色,B的水溶液呈碱性,且混合后只产生不溶于稀硝酸的白色沉淀及能使红色石蕊试纸变蓝的气体。
①B的化学式为__________________。
②A、B溶液混合后加热呈中性,反应的离子方程式为__________________________。
(2)若A的水溶液呈浅绿色,B的水溶液无色且其焰色反应为黄色。向A的水溶液中加入稀盐酸无明显现象,再加入B后溶液变黄,但A、B的水溶液混合亦无明显变化。则
①A为_______________。
②经分析上述过程中溶液变黄的原因可能有两种:
Ⅰ._______ _____________________。 Ⅱ.___________ ____________。
③请用一简易方法证明上述溶液变黄的原因__________________________________。
④利用溶液变黄原理,将其设计成原电池,若电子由a流向b,则b极的电极反应式为_______________________________________

 [Fe(SCN) ]2+。
[Fe(SCN) ]2+。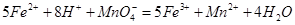 。准确称量上述药品10.00g,将其全部溶于试剂2中,配制成1000mL溶液,取出20.00mL,用0.0200mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00mL。
。准确称量上述药品10.00g,将其全部溶于试剂2中,配制成1000mL溶液,取出20.00mL,用0.0200mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00mL。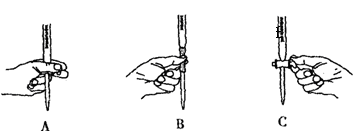
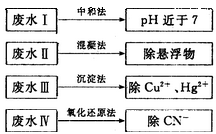
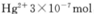 ,是否达到了排放标准_______(填“是”或“否”)。
,是否达到了排放标准_______(填“是”或“否”)。