��Ŀ����
��Ԫ��ʮ����Ҫ���䵥�ʼ��仯�����ڿ��С�������������ʮ�ֹ㷺����;��
��1����Ԫ�غ�������Ų�ʽΪ�� ��ԭ�Ӻ���� �ֲ�ͬ�ܼ��ĵ��ӣ���ԭ�Ӻ���������� �ֲ�ͬ����չ������ �ֲ�ͬ�˶�״̬�ĵ��ӡ�
��2�����¡��˹��̵������о����������³�ѹ�����������£�N2�ڴ���������ˮ������Ӧ��
2N2 (g)+6H2O (l) 4NH3 (g)+3O2 (g) - Q �������Ӧ��ƽ�ⳣ��Kֵ��÷�Ӧ ��ѡ���ţ���
4NH3 (g)+3O2 (g) - Q �������Ӧ��ƽ�ⳣ��Kֵ��÷�Ӧ ��ѡ���ţ���
A��һ��������Ӧ�����ƶ�
B����ƽ���ƶ�ʱ����Ӧ������������С
C��һ�����淴Ӧ�����ƶ�
D����ƽ���ƶ�ʱ�淴Ӧ�����ȼ�С������
��3�����������Ӧ�����������ܱ������н��У�����Ӧ�ﵽƽ��������жϴ������
A�������������ƽ������������ʱ����仯 B��ͨ�����ϡ����������߷�Ӧ������
C��������������ܶȲ���ʱ����仯 D��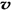 ��N2��/
��N2��/ 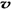 ��O2��=2:3
��O2��=2:3
��4�����������Ϊ���ȼ�ϵ���Ҫ�����塣��������ڸ�ѹ��450���������Ѹ�ٷֽ⣬��Ӧ�Ļ�ѧ����ʽ4NH4ClO4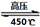 6H2O��+ 2N2��+ 4HCl��+ 5O2�����������������뻹ԭ��������ʵ���֮���� ��ÿ�ֽ�1mol������泥�ת�Ƶĵ�����Ŀ�� ��
6H2O��+ 2N2��+ 4HCl��+ 5O2�����������������뻹ԭ��������ʵ���֮���� ��ÿ�ֽ�1mol������泥�ת�Ƶĵ�����Ŀ�� ��
��1����Ԫ�غ�������Ų�ʽΪ�� ��ԭ�Ӻ���� �ֲ�ͬ�ܼ��ĵ��ӣ���ԭ�Ӻ���������� �ֲ�ͬ����չ������ �ֲ�ͬ�˶�״̬�ĵ��ӡ�
��2�����¡��˹��̵������о����������³�ѹ�����������£�N2�ڴ���������ˮ������Ӧ��
2N2 (g)+6H2O (l)
 4NH3 (g)+3O2 (g) - Q �������Ӧ��ƽ�ⳣ��Kֵ��÷�Ӧ ��ѡ���ţ���
4NH3 (g)+3O2 (g) - Q �������Ӧ��ƽ�ⳣ��Kֵ��÷�Ӧ ��ѡ���ţ���A��һ��������Ӧ�����ƶ�
B����ƽ���ƶ�ʱ����Ӧ������������С
C��һ�����淴Ӧ�����ƶ�
D����ƽ���ƶ�ʱ�淴Ӧ�����ȼ�С������
��3�����������Ӧ�����������ܱ������н��У�����Ӧ�ﵽƽ��������жϴ������
A�������������ƽ������������ʱ����仯 B��ͨ�����ϡ����������߷�Ӧ������
C��������������ܶȲ���ʱ����仯 D��
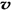 ��N2��/
��N2��/ 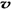 ��O2��=2:3
��O2��=2:3��4�����������Ϊ���ȼ�ϵ���Ҫ�����塣��������ڸ�ѹ��450���������Ѹ�ٷֽ⣬��Ӧ�Ļ�ѧ����ʽ4NH4ClO4
 6H2O��+ 2N2��+ 4HCl��+ 5O2�����������������뻹ԭ��������ʵ���֮���� ��ÿ�ֽ�1mol������泥�ת�Ƶĵ�����Ŀ�� ��
6H2O��+ 2N2��+ 4HCl��+ 5O2�����������������뻹ԭ��������ʵ���֮���� ��ÿ�ֽ�1mol������泥�ת�Ƶĵ�����Ŀ�� ����1�� 1s22s22P3 , 3, 4, 7
��2��AB
��3��B
��4�� 7��4 8NA �� 4.816��1024 ��
��2��AB
��3��B
��4�� 7��4 8NA �� 4.816��1024 ��
�����������1����Ԫ����7��Ԫ�غ��������7�����Ų�ʽΪ��1s22s22P3 �������������ܼ�����ԭ�Ӻ����3�ֲ�ͬ�ܼ��ĵ��ӣ���ԭ�Ӻ���������е���չ����s�����ε�ֻ��һ�֣�P�����3�֣�����4��չ��������ͬһ����ϵ�����������������ͬ���ʹ���7�ֲ�ͬ�˶�״̬�ĵ��ӡ�
��2��2N2 (g)+6H2O (l)
 4NH3 (g)+3O2 (g) - Q ������Ӧ�����ȷ�Ӧ�������Ӧ��ƽ�ⳣ��Kֵ�����������Ũ������Ӧ��Ũ�ȼ�С������ A��һ��������Ӧ�����ƶ�����ȷ��B����ƽ���ƶ�ʱ����Ӧ������������С��˵��ƽ�����ƣ���ȷ��
4NH3 (g)+3O2 (g) - Q ������Ӧ�����ȷ�Ӧ�������Ӧ��ƽ�ⳣ��Kֵ�����������Ũ������Ӧ��Ũ�ȼ�С������ A��һ��������Ӧ�����ƶ�����ȷ��B����ƽ���ƶ�ʱ����Ӧ������������С��˵��ƽ�����ƣ���ȷ����3���൱���ں��������У�A�������������ƽ������������ʱ����仯��˵���ﵽ��ƽ�⣬��ȷ�� B��ͨ�����ϡ����������ʵ���Ũ��û�иı䣬��Ӧ�����ʲ��ı䣬����C�����ڷ�Ӧǰ��������������ȣ�����������������ܶȲ���ʱ����仯������Ϊƽ���жϵ����ݣ���ȷ��D��
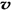 ��N2��/
��N2��/ 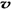 ��O2��=2:3������֮�ȵ��ڻ�ѧ������֮�ȣ���ȷ��
��O2��=2:3������֮�ȵ��ڻ�ѧ������֮�ȣ���ȷ����4���÷�Ӧ4NH4ClO4
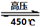 6H2O��+ 2N2��+ 4HCl��+ 5O2���У����������ǵ�������������ԭ�������Ȼ��⣬���ʵ���֮���� 7��4 ��ÿ�ֽ�1mol������泥�ת�Ƶĵ�����Ŀ�� 8NA �� 4.816��1024 ����
6H2O��+ 2N2��+ 4HCl��+ 5O2���У����������ǵ�������������ԭ�������Ȼ��⣬���ʵ���֮���� 7��4 ��ÿ�ֽ�1mol������泥�ת�Ƶĵ�����Ŀ�� 8NA �� 4.816��1024 ����
��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ


