题目内容
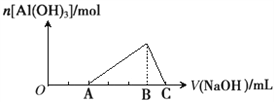
【题目】已知25℃时Ksp[Al(OH)3]=1.0×10-33,Ksp[Fe(OH)3]=4.0×10-38。向Fe(NO3)3和Al(NO3)3的混合溶液中逐滴加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积的关系如下图所示。计算表明当Fe3+完全沉淀时,Al3+恰好开始沉淀。下列说法正确的是 ( )
A. 原混合溶液中c(Fe3+):c(Al3+)=1:1
B. Fe(NO3)3溶液中混有杂质Al(NO3)3可以加入过量的NaOH溶液除去
C. B点两种沉淀共存,此时上层溶液中c(Al3+):c(Fe3+)=2.5×104
D. C点溶液中的溶质只有NaAlO2
【答案】C
【解析】当Fe3+完全沉淀时,Al3+恰好开始沉淀,所以OA段的反应是Fe3++3OH-= Fe(OH)3;AB段的反应是Al3++3OH-= Al(OH)3;BC段反应是Al(OH)3 +OH-=[Al(OH)4]-;OA段、AB段消耗氢氧化钠的比为2:3,所以原混合溶液中c(Fe3+):c(Al3+)=2:3,故A错误;Fe(NO3)3溶液中混有杂质Al(NO3)3,加入过量的NaOH溶液生成氢氧化铁沉淀,没有Fe(NO3)3,故B错误;B点两种沉淀共存,此时上层溶液中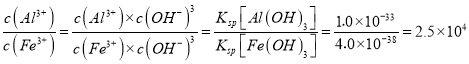 ,故C正确;C点溶液中的溶质有NaAlO2、NaNO3,故D错误。
,故C正确;C点溶液中的溶质有NaAlO2、NaNO3,故D错误。

练习册系列答案
相关题目

