题目内容
锂的化合物用途广泛。Li3N是非常有前途的储氢材料;LiFePO4、Li2FeSiO4等可以作为电池的正级材料。回答下列问题:
(1)将锂在纯氮气中燃烧可制得Li3N,其反应的化学方程为 。
(2)氮化锂在氢气中加热时可得到氨基锂(LiNH2),其反应的化学方程式为:
Li3N+2H2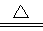 LiNH2+2LiH,氧化产物为 (填化学式)。在270℃时,该反应可逆向发生放出H2,因而氮化锂可作为储氢材料,储存氢气最多可达Li3N质量的 %(精确到0.1)。
LiNH2+2LiH,氧化产物为 (填化学式)。在270℃时,该反应可逆向发生放出H2,因而氮化锂可作为储氢材料,储存氢气最多可达Li3N质量的 %(精确到0.1)。
(3)将Li2CO3、FeC2O4·2H2O和SiO2粉末均匀混合,在800℃的氩气中烧结6小时制得Li2FeSiO4,写出反应的化学方程式 ,制备Li2FeSiO4的过程必须在惰性气体氛围中进行,其原因是 。
(4)将一定浓度磷酸二氢铵、氯化锂混合溶液作为电解液,以铁棒为阳极,石墨为阴极,电解析出LiFePO4沉淀,阳极的电极反应式为 。
(5)磷酸亚铁锂电池充放电过程中,发生LiFePO4与Li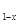 FePO4之间的转化,电池放电时负极发生的反应为LiXC6-Xe—
FePO4之间的转化,电池放电时负极发生的反应为LiXC6-Xe—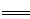 XLi++6C,写出电池放电时的电极反应的化学方程式 。
XLi++6C,写出电池放电时的电极反应的化学方程式 。
(1)将锂在纯氮气中燃烧可制得Li3N,其反应的化学方程为 。
(2)氮化锂在氢气中加热时可得到氨基锂(LiNH2),其反应的化学方程式为:
Li3N+2H2
 LiNH2+2LiH,氧化产物为 (填化学式)。在270℃时,该反应可逆向发生放出H2,因而氮化锂可作为储氢材料,储存氢气最多可达Li3N质量的 %(精确到0.1)。
LiNH2+2LiH,氧化产物为 (填化学式)。在270℃时,该反应可逆向发生放出H2,因而氮化锂可作为储氢材料,储存氢气最多可达Li3N质量的 %(精确到0.1)。(3)将Li2CO3、FeC2O4·2H2O和SiO2粉末均匀混合,在800℃的氩气中烧结6小时制得Li2FeSiO4,写出反应的化学方程式 ,制备Li2FeSiO4的过程必须在惰性气体氛围中进行,其原因是 。
(4)将一定浓度磷酸二氢铵、氯化锂混合溶液作为电解液,以铁棒为阳极,石墨为阴极,电解析出LiFePO4沉淀,阳极的电极反应式为 。
(5)磷酸亚铁锂电池充放电过程中,发生LiFePO4与Li
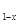 FePO4之间的转化,电池放电时负极发生的反应为LiXC6-Xe—
FePO4之间的转化,电池放电时负极发生的反应为LiXC6-Xe— XLi++6C,写出电池放电时的电极反应的化学方程式 。
XLi++6C,写出电池放电时的电极反应的化学方程式 。(1)6Li+N2 2Li3N
2Li3N
(2)LiNH2 11.4
(3)Li2CO3+FeC2O4?2H2O+SiO2 Li2FeSiO4+CO↑+CO2↑+2H2O
Li2FeSiO4+CO↑+CO2↑+2H2O
防止二价铁被氧化
(4)Fe+H2PO4-+Li+-2e-=LiFePO4+2H+
(5)Li1-xFePO4+LixC6=6C+LiFePO4
 2Li3N
2Li3N(2)LiNH2 11.4
(3)Li2CO3+FeC2O4?2H2O+SiO2
 Li2FeSiO4+CO↑+CO2↑+2H2O
Li2FeSiO4+CO↑+CO2↑+2H2O防止二价铁被氧化
(4)Fe+H2PO4-+Li+-2e-=LiFePO4+2H+
(5)Li1-xFePO4+LixC6=6C+LiFePO4
(1)锂与氮气在点燃条件下与氮气发生反应生成Li3N,该反应的化学方程式为:6Li+N2 2Li3N。
2Li3N。
(2)反应Li3N+2H2 LiNH2+2LiH中,锂元素、N元素化合价不变,氢气化合价由0变成+1价的LiNH2,化合价升高被氧化,所以氧化产物为LiNH2;该反应中,反应掉2mol氢气,同时消耗1mol氮化锂,所以储存氢气最多可达Li3N质量的:4/35×100%≈11.4%。
LiNH2+2LiH中,锂元素、N元素化合价不变,氢气化合价由0变成+1价的LiNH2,化合价升高被氧化,所以氧化产物为LiNH2;该反应中,反应掉2mol氢气,同时消耗1mol氮化锂,所以储存氢气最多可达Li3N质量的:4/35×100%≈11.4%。
(3)将Li2CO3、FeC2O4?2H2O和SiO2粉末均匀混合,在800℃的氩气中烧结6小时制得Li2FeSiO4,根据质量守恒、化合价升降相等可以判断,反应产物还会有一氧化碳、二氧化碳和水生成,该反应的化学方程式为:Li2CO3+FeC2O4?2H2O+SiO2 Li2FeSiO4+CO↑+CO2↑+2H2O;亚铁离子容易被氧化,所以该反应需要在惰性气体氛围中进行。
Li2FeSiO4+CO↑+CO2↑+2H2O;亚铁离子容易被氧化,所以该反应需要在惰性气体氛围中进行。
(4)电解池中阳极发生氧化反应,铁为阳极,所以阳极铁失去电子,与H2PO4-、Li+反应生成LiFePO4沉淀,发生的电极反应Fe+H2PO4-+Li+-2e-=LiFePO4+2H+
(5)磷酸亚铁锂电池充放电过程中,发生LiFePO4与Li1-xFePO4之间的转化,其中LiFePO4→Li1-xFePO4的转化化合价降低,发生还原反应,而电池放电时负极发生的反应为LixC6-xe-═xLi++6C,该反应为氧化反应,所以反应转化应该为:LiFePO4→Li1-xFePO4,所以电池放电时反应的化学方程式为:
Li1-xFePO4+LixC6=6C+LiFePO4。
 2Li3N。
2Li3N。(2)反应Li3N+2H2
 LiNH2+2LiH中,锂元素、N元素化合价不变,氢气化合价由0变成+1价的LiNH2,化合价升高被氧化,所以氧化产物为LiNH2;该反应中,反应掉2mol氢气,同时消耗1mol氮化锂,所以储存氢气最多可达Li3N质量的:4/35×100%≈11.4%。
LiNH2+2LiH中,锂元素、N元素化合价不变,氢气化合价由0变成+1价的LiNH2,化合价升高被氧化,所以氧化产物为LiNH2;该反应中,反应掉2mol氢气,同时消耗1mol氮化锂,所以储存氢气最多可达Li3N质量的:4/35×100%≈11.4%。(3)将Li2CO3、FeC2O4?2H2O和SiO2粉末均匀混合,在800℃的氩气中烧结6小时制得Li2FeSiO4,根据质量守恒、化合价升降相等可以判断,反应产物还会有一氧化碳、二氧化碳和水生成,该反应的化学方程式为:Li2CO3+FeC2O4?2H2O+SiO2
 Li2FeSiO4+CO↑+CO2↑+2H2O;亚铁离子容易被氧化,所以该反应需要在惰性气体氛围中进行。
Li2FeSiO4+CO↑+CO2↑+2H2O;亚铁离子容易被氧化,所以该反应需要在惰性气体氛围中进行。(4)电解池中阳极发生氧化反应,铁为阳极,所以阳极铁失去电子,与H2PO4-、Li+反应生成LiFePO4沉淀,发生的电极反应Fe+H2PO4-+Li+-2e-=LiFePO4+2H+
(5)磷酸亚铁锂电池充放电过程中,发生LiFePO4与Li1-xFePO4之间的转化,其中LiFePO4→Li1-xFePO4的转化化合价降低,发生还原反应,而电池放电时负极发生的反应为LixC6-xe-═xLi++6C,该反应为氧化反应,所以反应转化应该为:LiFePO4→Li1-xFePO4,所以电池放电时反应的化学方程式为:
Li1-xFePO4+LixC6=6C+LiFePO4。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
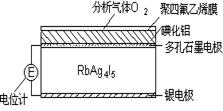


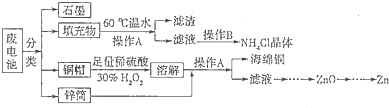


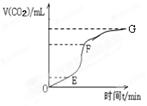

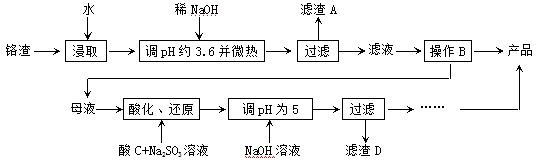
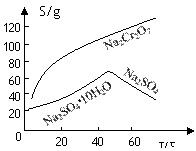
 Cr2O72-+H2O设计图示装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图中右侧电极连接电源的 极,其电极反应式为 。
Cr2O72-+H2O设计图示装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图中右侧电极连接电源的 极,其电极反应式为 。