题目内容
某氯化铁样品含有少FeC12杂质。现要测定其中铁元素的质量分数,实验按以下步骤进行: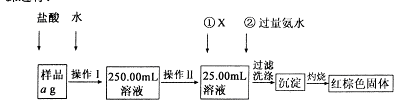
请根据上图流程,回答以下问题:
(1)操作Ⅰ所用到的玻璃仪器除烧杯、玻璃棒外,还必须有 、 (填仪器名称),操作Ⅱ必须用到的仪器是 (填编号)。
| A.50mL烧杯 | B.50mL量筒 | C.100mL量筒 | D.25mL酸式滴定管 |
(3)检验沉淀是否已经洗涤干净的操作是 。
(4)若蒸发皿质量是W1g,蒸发皿与加热后固体总质量W2g,则样品中铁元素的质量分数是 (列出计算式,不需化简):若固体加热时未充分反应,则最终测量的结果 (“偏大”、“偏小”、“不变”)。
(5)已知在常温下Cu2+和Fe3+在溶液中随pH变化时水解的曲线如图所示
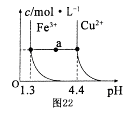 。
。对图中a点的说法正确的是 (填序号)。
①加适量NH4C1固体可使溶液由a点沿水平方向变到Cu2+曲线上。
②溶液中a点和水平线在Fe3+和Cu2+曲线上任意截点的C(H+)与c(OH-)乘积相等
③Fe(OH)3、Cu(OH)2在a点代表的溶液中均达到饱和
(14分)(1)250ml容量瓶(1分) 胶头滴管(1分); D(1分)
(2)H2O2或Cl2或HNO3等(1分);使Fe2+被氧化为Fe3+(1分);使Fe3+成分沉淀(1分)
(3)取少量最后一次洗出液,滴加AgNO3溶液,若无沉淀生成,则证明洗涤干净(其他合理答案均可)(2分)
(4)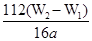 ×100%(2分);偏大(2分) (5)②(2分)
×100%(2分);偏大(2分) (5)②(2分)
解析试题分析:(1)操作Ⅰ是配制一定物质的量浓度溶液,所用到的玻璃仪器除烧杯、玻璃棒外,还必须有250ml容量瓶和胶头滴管。操作Ⅱ是量取25.00ml溶液,需要滴定管。溶液显书写需要酸式滴定管,答案选D。
(2)由于溶液中含有亚铁离子,需要将其氧化生成铁离子,所以X应该是氧化剂,可以选择H2O2或Cl2或HNO3等。由于要使溶液中的铁离子完全沉淀生成氢氧化铁,所以加入的氨水应该是过量的。
(3)由于沉淀表面含有Cl-,所以可以通过检验Cl-来检验沉淀是否洗涤干净,即取少量最后一次洗出液,滴加AgNO3溶液,若无沉淀生成,则证明洗涤干净。
(4)氢氧化铁分解生成氧化铁,则氧化铁的质量是(W2-W1)g,所以干净原子守恒可知,样品中铁元素的含量是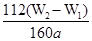 ×10×100%=
×10×100%=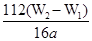 ×100%。若固体加热时未充分反应,则W2偏大,所以最终测量的结果偏大。
×100%。若固体加热时未充分反应,则W2偏大,所以最终测量的结果偏大。
(5)①、氯化铵固体溶于水,NH4+水解,溶液的酸性增强,pH降低,所以不可能使溶液由a点沿水平方向变到Cu2+曲线上,①不正确;②、温度不变,则溶液中水的离子积常数是不变的,②正确;③、a点均不在曲线上,其中铁离子已经完全沉淀,铜离子没有沉淀,是不饱和溶液,③不正确,答案选②。
考点:考查一定物质的量浓度的配制、仪器的选择、反应条件的控制、离子的检验、元素含量的测定与误差分析、离子积常数的应用与溶解平衡的判断等

 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案某化学实验小组想要了解市场所售食用白醋(主要是醋酸的水溶液)的准确浓度,现从市场上买来一瓶某品牌食用白醋,用实验室标准NaOH溶液对其进行滴定。
(1)该实验应选用 作指示剂,量取一定体积的白醋所用的仪器是 。
(2)如图表示50mL滴定管中液面的位置,若A与C刻度间相差1mL,A处的刻度为25,滴定管中液面读数应为 mL。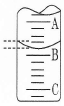
(3)为了减小实验误差,该同学一共进行了3次实验,假设每次所取白醋体积均为VmL,NaOH标准液浓度为cmo1/L,3次实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗NaOH溶液体积/mL | 26.02 | 25.35 | 25.30 |
从上表可以看出,第一次实验中记录消耗NaOH溶液的体积明显多于后两次,其原因可能是( )
A.初读正确,实验结束时俯视刻度线读取滴定终点时NaOH溶液的体积
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.盛装标准液的滴定管装液前用蒸馏水洗净,未用标准液润洗
D.滴加NaOH溶液过快,未充分振荡,刚看到溶液变色,立刻停止滴定
(4)白醋溶液中存在的电离平衡为 (用电离平衡方程式表示)。
(5)在滴定过程中,当c(CH3COOˉ)>c(Na+)时,则混合溶液呈____(填序号)。
A.酸性 B.碱性 C.中性 D.无法确定
(6)根据所给数据,写出计算该白醋中醋酸的物质的量浓度的表达式(不必化简):c= 。
下图是一种航天器能量储存系统原理示意图。下列说法正确的是( )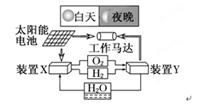
| A.该系统中只存在3种形式的能量转化 |
| B.装置Y中负极的电极反应式为:O2+2H2O+4e-=4OH- |
| C.装置X能实现燃料电池的燃料和氧化剂再生 |
| D.装置X、Y形成的子系统能实现物质的零排放,并能实现化学能与电能间的完全转化 |
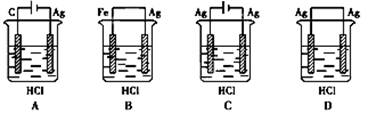
利用下图装置可以模拟铁的电化学防护。下列说法不正确的是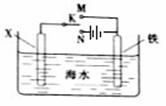
| A.若X为锌棒,开关K置于M处,可减缓铁的腐蚀 |
| B.若X为锌棒,开关K置于M处,铁极发生氧化反应 |
| C.若X为碳棒,开关K置于N处,可减缓铁的腐蚀 |
| D.若X为碳棒,开关K置于N处,X极发生氧化反应 |

 I—+ I2。实验室可以通过氧化还原滴定法测定平衡时I3—的浓度
I—+ I2。实验室可以通过氧化还原滴定法测定平衡时I3—的浓度