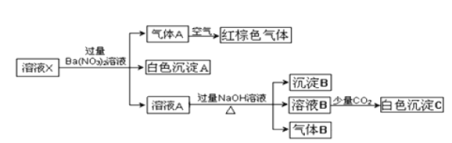
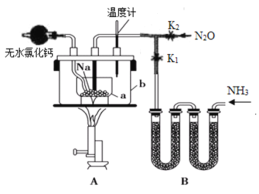
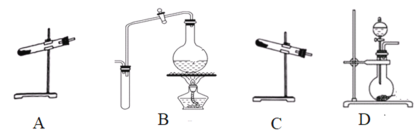
��Ŀ����
����Ŀ��25 ��ʱ����������ĵ��볣�����£�
����Ļ�ѧʽ | CH3COOH | HCN | H2S |
���볣��(25 ��) | 1.8��10��5 | 4.9��10��10 | K1��1.3��10��7 K2��7.1��10��15 |
25 ��ʱ������˵����ȷ����
A.�����ʵ���Ũ�ȵĸ���Һ��pH��ϵΪ��pH(CH3COONa)>pH(Na2S)>pH(NaCN)
B.a mol/L HCN��Һ��b mol/L NaOH��Һ�������ϣ�������Һ��c(Na��)>c(CN��)����aһ������b
C.NaHS��Na2S�Ļ����Һ�У�һ������c(Na��)��c(H��)��c(OH��)��c(HS��)��2c(S2��)
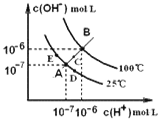
D.ijŨ�ȵ�HCN��Һ��pH��d��������c(OH��)��10��d mol/L
���𰸡�C
��������
A.�ɵ��볣��Ka�Ĺ�ϵ��֪��1.8��10-5��4.9��10-10��7.1��10-15��������CH3COOH��HCN��HS-����Ȼ��Ũ��ʱNa2S��ˮ��̶��������Һ��pH���������ʵ���Ũ�ȵĸ���ҺpH��ϵΪpH��Na2S����pH��NaCN����pH��CH3COONa������A����
B.��Һ�еĵ���غ㣺C��H+��+c��Na+��=c��CN-��+C��OH-������֪c��Na+����c��CN-������֪c��H+����c��OH-������Һ�ʼ��ԣ���a����С�ڻ����b����B����
C.������Һ�еĵ���غ㣬��֪NaHS��Na2S�Ļ����Һ�У�һ������c(Na��)��c(H��)��c(OH��)��c(HS��)��2c(S2��)����C��ȷ��
D. 25 ��ʱ��ijŨ�ȵ�HCN��Һ��pH��d��������c(OH��)��![]() 10d-14mol/L����D����
10d-14mol/L����D����
�ʴ�ѡC��

 ���ѵ����Ԫ��ĩ���100��ϵ�д�
���ѵ����Ԫ��ĩ���100��ϵ�д� ��˼άС�ھ�100����ҵ��ϵ�д�
��˼άС�ھ�100����ҵ��ϵ�д� ��ʦָ��һ��ͨϵ�д�
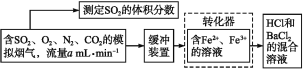
��ʦָ��һ��ͨϵ�д�����Ŀ���ϳɰ������Ĵ����������˹��̵�����Ҫ;�������о�������ȷ������ָ�����ϳɰ���Ӧ��ƽ�ⳣ��Kֵ���¶ȵĹ�ϵ�����
�� �ȣ��棩 | 360 | 440 | 520 |
Kֵ | 0.036 | 0.010 | 0.0038 |
��1�������ϱ����ݿ�֪�÷�ӦΪ_____ ������ȣ����ȣ���ȷ��������Ӧ��
�����д�ʩ������������ԭ��������_____������ţ���
a������ѹǿ�����ںϳɰ� b��ʹ�ú��ʵĴ��������ڿ������ɰ�
c����������Ҫ�����¶���500��C���� d����Ҫʹ�ù�����N2�����H2ת����
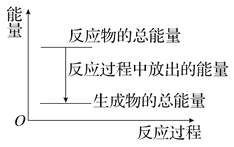
��2��0.2mol��������ˮ�����뺬��0.2mol�������Һ��Ӧ����QkJ���������Ȼ�ѧ����ʽ��ʾ�䷴Ӧʽ_____��
��3������ʱ����amol��������ˮ����ͨ��bmol�Ȼ��⣬��Һ���Ϊ1L����c��NH4+��=c��Cl��������һˮ�ϰ��ĵ���ƽ�ⳣ��Kb=_____����ab��ʾ����
��4��ԭ����H2��ͨ����Ӧ CH4��g��+H2O ��g��![]() CO��g��+3H2��g�� ��ȡ����֪�÷�Ӧ�У�����ʼ������е�
CO��g��+3H2��g�� ��ȡ����֪�÷�Ӧ�У�����ʼ������е�![]() �㶨ʱ���¶ȡ�ѹǿ��ƽ������CH4������Ӱ����ͼ��ʾ��
�㶨ʱ���¶ȡ�ѹǿ��ƽ������CH4������Ӱ����ͼ��ʾ��
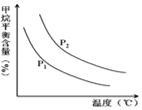
��ͼ�У��������߱�ʾѹǿ�Ĺ�ϵ�ǣ�P1_____P2�����������=����������
����������һ���������¶ȣ������IJ��ʻ�__�����������С����С�������䡱���䣩��
��5��ԭ����H2����ͨ����ӦCO��g��+H2O��g��![]() CO2��g��+H2��g����ȡ��
CO2��g��+H2��g����ȡ��
��T��ʱ�����ݻ��̶�Ϊ5L�������г���1molˮ������1mol CO����Ӧ��ƽ����CO��Ũ��Ϊ0.08molL��1�����¶��·�Ӧ��ƽ�ⳣ��KֵΪ_____��
�ڱ����¶���ΪT�����ݻ����Ϊ5L���ı�ˮ������CO�ij�ʼ���ʵ���֮�ȣ������������з�Ӧ�����������ܹ�˵����ϵ����ƽ��״̬����_____������ţ���
a��������ѹǿ����ʱ��ı�
b�����������ܶȲ���ʱ��ı�
c����λʱ��������a mol CO2��ͬʱ����a mol H2
d���������n��CO����n��H2O����n��CO2����n��H2��=1��16��6��6