题目内容
 如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:(1)该浓盐酸的物质的量浓度为
12.0
12.0
mol/L.(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是
BD
BD
.A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制450mL物质的量浓度为0.3mol/L稀盐酸.
①需要使用的主要仪器有量筒、烧杯、玻璃棒、
500ml容量瓶
500ml容量瓶
、胶头滴管
胶头滴管
.②其操作步骤可分解为以下几步:
A.用量筒量取
12.5
12.5
mL浓盐酸,缓缓注入装有约50mL蒸馏水的烧杯里,并用玻璃棒搅拌.B.用适量蒸馏水分三次洗涤烧杯和玻璃棒,将每次的洗液都移入容量瓶里.
C.将稀释后的盐酸小心地用玻璃棒引流到容量瓶里.
D.检查容量瓶是否漏水.
E.将蒸馏水直接加入容量瓶,至液面接近刻度线1-2cm处.
F.盖紧瓶塞,反复颠倒振荡,摇匀溶液.
G.用胶头滴管向容量瓶里逐滴加入蒸馏水,到液面最低点恰好与刻线相切.
完成上述步骤中的空白处.
③补充完成正确的操作顺序(用字母填写):
( D )→( A )→( C )→
B
B
→E
E
→G
G
→( F ).(4)在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?
(在括号内填“偏高”或“偏低”或“无影响”).
①用量筒量取浓盐酸时俯视观察凹液面
偏低
偏低
②定容时,眼睛俯视刻度线,
偏高
偏高
③定容后,加盖倒转摇匀后,发现溶面低于刻度线,又滴加蒸馏水至刻度.
偏低
偏低
.分析:(1)根据c=
计算出该浓盐酸的物质的量浓度;
(2)任何溶液都是均一稳定的分散系,任何体积的密度和浓度不变;
(3)①根据配制一定物质的量浓度的溶液的配制步骤选择使用仪器;
②A、配制450mL溶液,需要配制500mL溶液,根据500mL 0.3mol/L稀盐酸中氯化氢的物质的量计算出需要浓盐酸的体积;
③根据配制一定物质的量浓度的溶液配制步骤进行排序;
(4)根据c=
可得,一定物质的量浓度溶液配制的误差都是由溶质的物质的量n和溶液的体积V引起的,误差分析时,关键要看配制过程中引起n和V怎样的变化;若n比理论值小,或V比理论值大时,都会使所配溶液浓度偏小;若n比理论值大,或V比理论值小时,都会使所配溶液浓度偏大.
| 1000ρw |
| M |
(2)任何溶液都是均一稳定的分散系,任何体积的密度和浓度不变;
(3)①根据配制一定物质的量浓度的溶液的配制步骤选择使用仪器;
②A、配制450mL溶液,需要配制500mL溶液,根据500mL 0.3mol/L稀盐酸中氯化氢的物质的量计算出需要浓盐酸的体积;
③根据配制一定物质的量浓度的溶液配制步骤进行排序;
(4)根据c=
| n |
| V |
解答:解:(1)该盐酸的物质的量浓度为:c=
mol/L=12.0mol/L,
故答案为:12.0;
(2)任何溶液都是均一稳定的分散系,任何体积的密度和浓度不变,而体积不同时,溶质的物质的量不同,溶液中离子的数目也不同,
故答案为:BD;
(3)配制450mL物质的量浓度为0.3mol/L稀盐酸,实验室没有450mL容量瓶,所以需要选用500mL容量瓶,配制的溶液体积为500mL,
①配制溶液时,操作步骤为:计算、量取、溶解、移液、洗涤、定容、摇匀等操作,需要使用的主要仪器有量筒、烧杯、玻璃棒、500mL容量瓶、胶头滴管,
故答案为:500ml容量瓶;胶头滴管;
②配制500mL 0.3mol/L的稀盐酸,需要12.0mol/L的体积为:
=0.0125L=12.5mL,
故答案为:12.5;
③配制500mL 0.3mol/L的稀盐酸,操作步骤为:计算、量取、溶解、移液、洗涤、定容、摇匀等操作,所以操作顺序为:DACBEG,
故选BEG;
(4)①用量筒量取浓盐酸时俯视观察凹液面,导致量取的浓盐酸体积偏小,根据c=
可得,配制的溶液浓度偏低,
故答案为:偏低;
②定容时,眼睛俯视刻度线,导致加入的蒸馏水体积偏小,根据c=
可得,配制的溶液浓度偏高,
故答案为:偏高;
③定容后,加盖倒转摇匀后,发现溶面低于刻度线,又滴加蒸馏水至刻度,导致配制的溶液体积偏大,根据c=
可得,配制的溶液浓度偏低,
故答案为:偏低.
| 1000×1.2×36.5% |
| 36.5 |
故答案为:12.0;
(2)任何溶液都是均一稳定的分散系,任何体积的密度和浓度不变,而体积不同时,溶质的物质的量不同,溶液中离子的数目也不同,
故答案为:BD;
(3)配制450mL物质的量浓度为0.3mol/L稀盐酸,实验室没有450mL容量瓶,所以需要选用500mL容量瓶,配制的溶液体积为500mL,
①配制溶液时,操作步骤为:计算、量取、溶解、移液、洗涤、定容、摇匀等操作,需要使用的主要仪器有量筒、烧杯、玻璃棒、500mL容量瓶、胶头滴管,
故答案为:500ml容量瓶;胶头滴管;
②配制500mL 0.3mol/L的稀盐酸,需要12.0mol/L的体积为:
| 0.3mol/L×0.5L |
| 12.0mol/L |
故答案为:12.5;
③配制500mL 0.3mol/L的稀盐酸,操作步骤为:计算、量取、溶解、移液、洗涤、定容、摇匀等操作,所以操作顺序为:DACBEG,
故选BEG;
(4)①用量筒量取浓盐酸时俯视观察凹液面,导致量取的浓盐酸体积偏小,根据c=
| n |
| V |
故答案为:偏低;
②定容时,眼睛俯视刻度线,导致加入的蒸馏水体积偏小,根据c=
| n |
| V |
故答案为:偏高;
③定容后,加盖倒转摇匀后,发现溶面低于刻度线,又滴加蒸馏水至刻度,导致配制的溶液体积偏大,根据c=
| n |
| V |
故答案为:偏低.
点评:本题考查了配制一定物质的量浓度的溶液的方法,该题是中等难度的试题,试题基础性强,该题难易适中,注重灵活性,侧重对学生能力的培养和解题方法的指导和训练,有利于培养学生的逻辑思维能力和严谨的规范实验操作能力;该题的难点在于误差分析,根据验操作对c=
产生的影响判断.
| n |
| V |

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
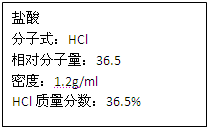 如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
 如图为实验室某浓盐酸试剂瓶的标签上的有关数据,试回答下列问题:
如图为实验室某浓盐酸试剂瓶的标签上的有关数据,试回答下列问题: 如图为实验室某浓盐酸试剂瓶上的标签的有关内容,试根据标签上的有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶上的标签的有关内容,试根据标签上的有关数据回答下列问题: