题目内容
【题目】二氧化钛广泛应用于各类结构表面涂料、纸张涂层等,二氧化钛还可作为制备钛单质的原料。现在工业由以下两种方法制备二氧化钛:
方法1:可用含有Fe2O3、SiO2的钛铁矿(主要成分为FeTiO3,其中Ti元素化合价为+4价)制取,其主要工艺流程如下:
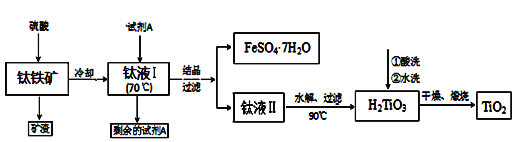
已知有关反应包括:
酸溶FeTiO3(s)+2H2SO4(aq)→FeSO4(aq)+TiOSO4(aq)+2H2O(l)
水解TiOSO4(aq)+2H2O(l)→H2TiO3(s)+H2SO4(aq)
(1)试剂A为____,钛液Ⅰ需冷却至70℃左右,若温度过高会导致产品收率降低,原因____;
(2)取少量酸洗后的H2TiO3,加入盐酸并振荡,滴加KSCN溶液后无明显现象,再加H2O2后出现红色,说明H2TiO3中存在的杂质离子是__________。这种H2TiO3即使用水充分洗涤,煅烧后获得的TiO2会略发黄,发黄的杂质是_____________(填化学式)。
方法2:
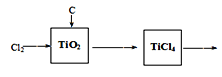
Ⅰ.将干燥后的金红石(主要成分TiO2,主要杂质SiO2)与碳粉混合装入氯化炉中,在高温下通入Cl2反应制得混有SiCl4杂质的TiCl4;
II.将SiCl4分离,得到纯净的TiCl4;
III.在TiCl4中加水、加热,水解得到沉淀TiO2·xH2O,洗涤和干燥;
IV.TiO2·xH2O高温分解得到TiO2。
(1)TiCl4水解生成TiO2x H2O的化学方程式为____________________;
(2)检验TiO2x H2O中Cl-是否被除净的方法是____________________;金属钛被称为“21世纪金属”,工业制备金属钛是在800~900℃及惰性气体的保护下,在密闭反应器中,将TiCl4以一定的流速通入熔化的镁即可。主要涉及以下反应:
①TiO2+2Cl2+C→TiCl4+CO2
②TiCl4+2Mg → 2MgCl2+Ti
(3)下列推断不合理的是________
A.钛在高温下可能易与氧气反应
B.镁的熔点比钛的熔点高
C.钛的金属活动性比镁的金属活动性强
D.反应②产生的MgCl2可作为电解法制取镁的原料
(4)请完成以TiO2、Cl2和焦炭为原料制取金属Ti和Mg的流程图,并用箭头标明物料循环。___________________
【答案】铁粉 由于TiOSO4容易水解,若温度过高,则会有较多TiOSO4水解为固体H2TiO3而经过滤进入FeSO4·7H2O中导致TiO2产率降低 Fe2+ Fe2O3 TiCl4+(2+x)H2O![]() TiO2xH2O↓+4HCl 取少量水洗液,滴加硝酸酸化AgNO3溶液,若不产生白色沉淀,说明Cl-已除净 BC
TiO2xH2O↓+4HCl 取少量水洗液,滴加硝酸酸化AgNO3溶液,若不产生白色沉淀,说明Cl-已除净 BC 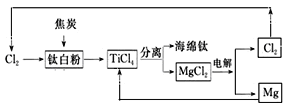
【解析】
含有Fe2O3、SiO2的钛铁矿(主要成分为FeTiO3,其中Ti元素化合价为+4价)加硫酸,在90℃温度下,溶解,过滤,滤液中含有FeSO4(aq)、TiOSO4(aq)和Fe2(SO4)3(aq),加铁粉(试剂A),把三价铁离子还原为亚铁离子,降温到70℃,结晶过滤,得到硫酸亚铁晶体,滤液为TiOSO4(aq),滤液温度升高到90℃,使TiOSO4水解生成H2TiO3固体,洗涤、干燥、煅烧得到TiO2。
(1)由流程可知Fe2(SO4)3与Fe粉反应产生FeSO4(aq),试剂A应为铁粉;由题中信息可知,TiOSO4容易水解,升高温度促进水解,若温度过高,则会有较多TiOSO4水解为固体H2TiO3而经过滤进入FeSO47H2O中导致TiO2产率降低;
(2)取少量酸洗后的H2TiO3,加入盐酸并振荡,滴加KSCN溶液后无明显现象,说明没有Fe3+,再加H2O2后出现红色,说明有Fe3+,则原来含有Fe2+,加H2O2后Fe2+被氧化为Fe3+;H2TiO3中的二价铁易被氧化为三价铁,煅烧时会生成Fe2O3,TiO2含有少量的Fe2O3会呈现黄色;
(1)设TiCl4的系数为1,根据元素守恒,TiO2xH2O的系数为1,HCl的系数为4;再根据O元素守恒,可知H2O的系数为(2+x),方程式为TiCl4+(2+x)H2O![]() TiO2xH2O↓+4HCl;
TiO2xH2O↓+4HCl;
(2)沉淀吸附溶液中的Cl-,根据发生反应:Cl-+Ag+=AgCl↓,可知检验TiO2x H2O中Cl-是否被除净的方法是:取最后一次的少量洗涤液,滴加硝酸酸化的AgNO3溶液,不产生白色沉淀,说明Cl-已除净;
(3)A. 工业制备金属钛是在800~900℃及惰性气体的保护下,说明钛在高温下可能易与氧气反应生成二氧化钛,A正确;
B. 镁易熔化熔点较低,镁的熔点比钛的熔点低,故B错误;
C. 活泼性强的金属能置换活泼性弱的金属,Mg能置换Ti,说明Mg比Ti活泼,C错误;
D. 电解熔融的MgCl2能制取镁,所以反应②产生的MgCl2可作为电解法制取镁的原料,故D正确;
故合理选项是BC;
(4)TiO2、Cl2和焦炭在高温条件下生成TiCl4和CO2,再用Mg单质置换TiCl4得到Ti和MgCl2,电解熔融的氯化镁又能得到Mg和Cl2,则以TiO2、Cl2和焦炭为原料制取金属Ti和Mg的流程图为: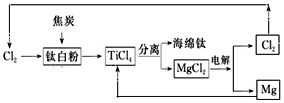 。
。