题目内容
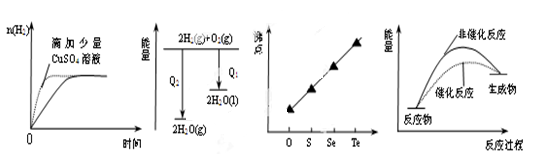
(1)短周期某主族元素M的电离能情况如图A所示.则M元素位于周期表的第______族.

(2)图B是研究部分元素的氢化物的沸点变化规律的图象,折线c可以表达出第______族元素氢化物的沸点的变化规律,①②③中表示为SiH4的是______
(3)不同同学对某主族元素氢化物的沸点的变化趋势画出了两条折线--折线a和折线b,你认为正确的是:______,理由是:______.
(4)有三种固态物质,它们的性质如下:
A物质:无色晶体,熔点3550℃,不导电,质硬,难溶于水及有机溶剂.
B物质:无色晶体,溶于水,质硬而脆,熔点800℃,熔化时能导电.
C物质:熔点-56.6℃,微溶于水,硬度小,固态或液态时不导电.
根据上述性质,可推断A和B的晶体类型为:A为______晶体,B为______晶体.

(2)图B是研究部分元素的氢化物的沸点变化规律的图象,折线c可以表达出第______族元素氢化物的沸点的变化规律,①②③中表示为SiH4的是______
(3)不同同学对某主族元素氢化物的沸点的变化趋势画出了两条折线--折线a和折线b,你认为正确的是:______,理由是:______.
(4)有三种固态物质,它们的性质如下:
A物质:无色晶体,熔点3550℃,不导电,质硬,难溶于水及有机溶剂.
B物质:无色晶体,溶于水,质硬而脆,熔点800℃,熔化时能导电.
C物质:熔点-56.6℃,微溶于水,硬度小,固态或液态时不导电.
根据上述性质,可推断A和B的晶体类型为:A为______晶体,B为______晶体.
(1)电离能是元素的原子失去电子所需要的能量,根据图象可以知道,元素的第三电离能之后数据相当大,说明易失去三个电子,最外层电子数为3,故为第ⅢA的元素,故答案为:IIIA;
(2)图B中元素的氢化物的沸点变化规律的图象中,折线c可以得出该族元素的氢化物的沸点随着原子序数的递增,从上到下是逐渐升高的,符合第IVA元素的性质,没有特例出现,折线c中①的沸点最低相对分子量最小为甲烷,所以②是SiH4,故答案为:IVA;②;
(3)A点氢化物的沸点为100℃,所以A点所示的氢化物是水,在水中,由于在水分子间存在氢键,其沸点高于氧族元素中的其它氢化物的沸点,即曲线b符合要求;故答案为:b;A点所示的氢化物是水,由于在水分子间存在氢键,所以其沸点高于氧族元素中的其它氢化物的沸点;
(4)A物质:无色晶体,熔点3550℃,不导电,质硬,难溶于水及有机溶剂,具有原子晶体的性质,属于原子晶体.
B物质:无色晶体,溶于水,质硬而脆,熔点800℃,熔化时能导电,具有离子晶体的性质,属于离子晶体.
C物质:熔点-56.6℃,微溶于水,硬度小,固态或液态时不导电,具有分子晶体的性质,属于分子晶体.
故答案为:原子;离子.
(2)图B中元素的氢化物的沸点变化规律的图象中,折线c可以得出该族元素的氢化物的沸点随着原子序数的递增,从上到下是逐渐升高的,符合第IVA元素的性质,没有特例出现,折线c中①的沸点最低相对分子量最小为甲烷,所以②是SiH4,故答案为:IVA;②;
(3)A点氢化物的沸点为100℃,所以A点所示的氢化物是水,在水中,由于在水分子间存在氢键,其沸点高于氧族元素中的其它氢化物的沸点,即曲线b符合要求;故答案为:b;A点所示的氢化物是水,由于在水分子间存在氢键,所以其沸点高于氧族元素中的其它氢化物的沸点;
(4)A物质:无色晶体,熔点3550℃,不导电,质硬,难溶于水及有机溶剂,具有原子晶体的性质,属于原子晶体.
B物质:无色晶体,溶于水,质硬而脆,熔点800℃,熔化时能导电,具有离子晶体的性质,属于离子晶体.
C物质:熔点-56.6℃,微溶于水,硬度小,固态或液态时不导电,具有分子晶体的性质,属于分子晶体.
故答案为:原子;离子.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案
相关题目