题目内容
下列反应达到平衡后,升高温度可以使混合气体平均相对分子质量增大的是( )
A.H2(g)+I2(g)  2HI(g) ΔH<0 2HI(g) ΔH<0 |
B.4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ΔH<0 4NO(g)+6H2O(g) ΔH<0 |
C.N2(g)+3H2(g)  2NH3(g)ΔH<0 2NH3(g)ΔH<0 |
D.2SO3(g) 2SO2(g)+O2(g) ΔH>0 2SO2(g)+O2(g) ΔH>0 |
B
试题分析:A.混合气体的总质量不变,总的物质的量不变,平均相对分子质量始终不变,A不符合;B.混合气体的总质量不变,温度升高平衡向逆反应方向移动,混合气体总的物质的量减小,平均相对分子质量增大,B符合;C.混合气体的总质量不变,温度升高平衡向逆反应方向移动,混合气体总的物质的量增大,平均相对分子质量减小,C不符合;D.混合气体的总质量不变,温度升高平衡向逆反应正反应方向移动,混合气体总的物质的量增大,平均相对分子质量减小,D不符合;选B.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
 2C(g)达到平衡的标志的是
2C(g)达到平衡的标志的是 xC(g),达平衡后,C在平衡混合气中的体积分数为w。若维持温度不变,按1.2molA、0.4molB、0.6molC为起始物质,达平衡后压强不变,C的体积分数仍为w,则x的值为
xC(g),达平衡后,C在平衡混合气中的体积分数为w。若维持温度不变,按1.2molA、0.4molB、0.6molC为起始物质,达平衡后压强不变,C的体积分数仍为w,则x的值为 Y(g)+Z(s),以下能说明反应达到平衡标志的是( )
Y(g)+Z(s),以下能说明反应达到平衡标志的是( ) 4NO(g)+6H2O(g),下列叙述中正确的是
4NO(g)+6H2O(g),下列叙述中正确的是 2NH3(g) △H<0 。反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题:
2NH3(g) △H<0 。反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题: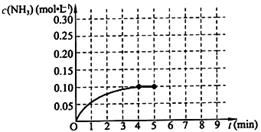
 H2(g)+CO2(g)平衡常数随温度的变化如下表:
H2(g)+CO2(g)平衡常数随温度的变化如下表: Cu2+ (aq) + 2Ag (s)设计成原电池,某一时刻的电子流向及电流计(G)指针偏转方向如图所示,有关叙述正确的是
Cu2+ (aq) + 2Ag (s)设计成原电池,某一时刻的电子流向及电流计(G)指针偏转方向如图所示,有关叙述正确的是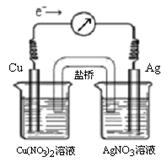
 N2(g)+CO2(g)+2H2O(g) ΔH=?867 kJ·mol-1。该反应可用于消除氮氧化物的污染。在130℃和180℃时,分别将0.50 molCH4和a molNO2充入1L的密闭容器中发生反应,测得有关数据如下表:
N2(g)+CO2(g)+2H2O(g) ΔH=?867 kJ·mol-1。该反应可用于消除氮氧化物的污染。在130℃和180℃时,分别将0.50 molCH4和a molNO2充入1L的密闭容器中发生反应,测得有关数据如下表: