题目内容
【题目】用NA表示阿伏加德罗常数的值.下列判断正确的是( )
A.32克O2和O3组成的混合气体中含有的氧原子数目为2NA
B.常温常压下,22.4 L乙醇含有的分子数目为NA
C.1 mol Na变为Na+时得到的电子数目为NA
D.44克14C16O2含氧原子数为2NA
【答案】A
【解析】解:A.氧气和臭氧均由氧原子构成,故32g混合气体中含有的氧原子的物质的量n= ![]() =
= ![]() =2mol,所以氧原子的数目为N=n×NA=2NA , 故A正确;
=2mol,所以氧原子的数目为N=n×NA=2NA , 故A正确;
B.常温常压下,气体摩尔体积大于22,4L/mol,所以22.4 L乙醇物质的量小于1mol,含有的分子数目小于NA , 故B错误;
C.1 mol Na变为Na+时失去的电子数目为NA , 故C错误;
D.物质的量n= ![]() =
= ![]() ,1mol14C16O2含2molO原子,44克14C16O2含氧原子数=
,1mol14C16O2含2molO原子,44克14C16O2含氧原子数= ![]() ×2×NA<2NA , 故D错误;
×2×NA<2NA , 故D错误;
故选A.

 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案【题目】CO是火力发电厂释放出的主要尾气,为减少对环境污染,发电厂试图采用CO与Cl2在催化剂的作用下合成光气(COCl2).某温度下,向2L的密闭容器中投入一定量的CO和Cl2 , 在催化剂的作用下发生反应:CO(g)+Cl2(g)COCl2(g)△H=a kJ/mol
反应过程中测定的部分数据如下表:
t/min | n (CO)/mol | n (Cl2)/mol |
0 | 1.20 | 0.60 |
1 | 0.90 | |
2 | 0.80 | |
4 | 0.20 |
(1)反应0~2min末的平均速率v(COCl2)=mol/(Lmin).
(2)在2min~4min间,v(Cl2)正v(Cl2)逆 (填“>”、“=”或“<”),该温度下K= .
(3)在图1中画出0~4min末n(COCl2)随时间的变化示意图 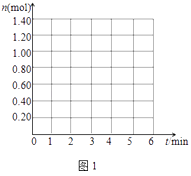
(4)已知X、L可分别代表温度或压强,如图2表示L一定时,CO的转化率随X的变化关系.X代表的物理量是;a0 (填“>”,“=”,“<”),依据是 

