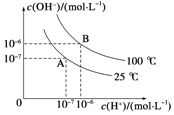
ЬтФПФкШн
ЁОЬтФПЁПЙІФмИпЗжзгЪЧжИОпгаФГаЉЬиЖЈЙІФмЕФИпЗжзгВФСЯЁЃЙІФмИпЗжзг P ЕФКЯГЩТЗЯпШчЯТЃК
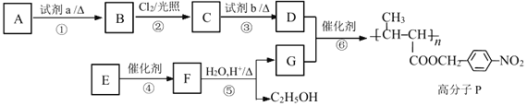
ЃЈ1ЃЉA ЪЧМзБНЃЌЪдМС a ЪЧ______ЁЃЗДгІЂлЕФЗДгІРраЭЮЊ______ЗДгІЁЃ
ЃЈ2ЃЉЗДгІЂкжа C ЕФВњТЪЭљЭљЦЋЕЭЃЌЦфдвђПЩФмЪЧ______ЁЃ
ЃЈ3ЃЉЗДгІЂоЕФЛЏбЇЗНГЬЪНЮЊ______ЁЃ
ЃЈ4ЃЉE ЕФЗжзгЪНЪЧ C6H10O2ЃЌЦфНсЙЙМђЪНЪЧ______ЁЃ
ЃЈ5ЃЉЮќЫЎДѓЭѕОлБћЯЉЫсФЦ![]() ЪЧвЛжжаТаЭЙІФмИпЗжзгВФСЯЃЌЪЧЁАФђВЛЪЊЁБЕФжївЊГЩЗжЁЃЙЄвЕЩЯгУБћЯЉЃЈCH2=CH-CH3ЃЉЮЊдСЯРДжЦБИОлБћЯЉЫсФЦЃЌЧыАбИУКЯГЩТЗЯпВЙГфЭъећЃЈЮоЛњЪдМСШЮбЁЃЉЁЃ_________
ЪЧвЛжжаТаЭЙІФмИпЗжзгВФСЯЃЌЪЧЁАФђВЛЪЊЁБЕФжївЊГЩЗжЁЃЙЄвЕЩЯгУБћЯЉЃЈCH2=CH-CH3ЃЉЮЊдСЯРДжЦБИОлБћЯЉЫсФЦЃЌЧыАбИУКЯГЩТЗЯпВЙГфЭъећЃЈЮоЛњЪдМСШЮбЁЃЉЁЃ_________
ЃЈКЯГЩТЗЯпГЃгУЕФБэДяЗНЪНЮЊЃКA![]() B
B![]() ЁЁФПБъВњЮяЃЉ
ЁЁФПБъВњЮяЃЉ
CH2=CH-CH3![]() CH2=CH-CH2Cl
CH2=CH-CH2Cl
ЁОД№АИЁПХЈСђЫсКЭХЈЯѕЫс ШЁДњ ИБВњЮяНЯЖрЃЌЕМжТВњЮяНЯЖрЃЌФПБъВњЮяВњТЪНЯЕЭ ![]() +nH2O CH3CH=CHCOOCH2CH3
+nH2O CH3CH=CHCOOCH2CH3 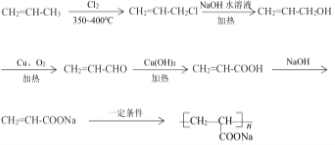
ЁОНтЮіЁП
AЮЊМзБНЃЌЦфНсЙЙМђЪНЪЧ![]() ЃЌНсКЯPЕФНсЙЙМђЪНЃЌПЩжЊAгыХЈЯѕЫсдкХЈСђЫсЁЂМгШШЬѕМўЯТЗЂЩњШЁДњЗДгІЩњГЩBЮЊ
ЃЌНсКЯPЕФНсЙЙМђЪНЃЌПЩжЊAгыХЈЯѕЫсдкХЈСђЫсЁЂМгШШЬѕМўЯТЗЂЩњШЁДњЗДгІЩњГЩBЮЊ![]() ЃЌBгыТШЦјдкЙтееЬѕМўЯТЗЂЩњШЁДњЗДгІЩњГЩCЮЊ
ЃЌBгыТШЦјдкЙтееЬѕМўЯТЗЂЩњШЁДњЗДгІЩњГЩCЮЊ![]() ЃЌCдкЧтбѕЛЏФЦЫЎШмвКЁЂМгШШЬѕМўЯТЗЂЩњЫЎНтЗДгІЩњГЩDЮЊ
ЃЌCдкЧтбѕЛЏФЦЫЎШмвКЁЂМгШШЬѕМўЯТЗЂЩњЫЎНтЗДгІЩњГЩDЮЊ![]() ЃЌПЩжЊGЕФНсЙЙМђЪНЮЊ
ЃЌПЩжЊGЕФНсЙЙМђЪНЮЊ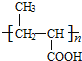 ЃЌдђFЮЊ
ЃЌдђFЮЊ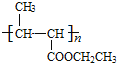 ЃЌEЕФЗжзгЪНЪЧC6H10O2ЃЌдђEЮЊCH3CH=CHCOOCH2CH3ЃЌвдДЫНтД№ИУЬтЁЃ
ЃЌEЕФЗжзгЪНЪЧC6H10O2ЃЌдђEЮЊCH3CH=CHCOOCH2CH3ЃЌвдДЫНтД№ИУЬтЁЃ
ЃЈ1ЃЉЗДгІЂйЪЧ![]() гыХЈЯѕЫсдкХЈСђЫсЁЂМгШШЬѕМўЯТЗЂЩњШЁДњЗДгІЩњГЩ
гыХЈЯѕЫсдкХЈСђЫсЁЂМгШШЬѕМўЯТЗЂЩњШЁДњЗДгІЩњГЩ![]() ЃЌЪдМСaЪЧЃКХЈСђЫсКЭХЈЯѕЫсЃЌЗДгІЂлЮЊТШДњЬўЕФШЁДњЗДгІЃЌ
ЃЌЪдМСaЪЧЃКХЈСђЫсКЭХЈЯѕЫсЃЌЗДгІЂлЮЊТШДњЬўЕФШЁДњЗДгІЃЌ
ЙЪД№АИЮЊЃКХЈСђЫсКЭХЈЯѕЫсЃЛШЁДњЃЛ
ЃЈ2ЃЉЙтееЬѕМўЯТЃЌТШЦјПЩШЁДњМзЛљЕФHдзгЃЌИБВњЮяНЯЖрЃЌЕМжТВњЮяНЯЖрЃЌФПБъВњЮяВњТЪНЯЕЭЃЌ
ЙЪД№АИЮЊЃКИБВњЮяНЯЖрЃЌЕМжТВњЮяНЯЖрЃЌФПБъВњЮяВњТЪНЯЕЭЃЛ
ЃЈ3ЃЉЗДгІЂоЕФЛЏбЇЗНГЬЪНЮЊ![]() ЃЌ
ЃЌ
ЙЪД№АИЮЊЃК![]() ЃЛ
ЃЛ
ЃЈ4ЃЉгЩвдЩЯЗжЮіПЩжЊEЮЊCH3CH=CHCOOCH2CH3ЃЌ
ЙЪД№АИЮЊЃКCH3CH=CHCOOCH2CH3ЃЛ
ЃЈ5ЃЉБћЯЉгыТШЦјдкМгШШЬѕМўЯТЗЂЩњШЁДњЗДгІЩњГЩCH2=CHCH2ClЃЌCH2=CHCH2ClЫЎНтЩњГЩCH2=CHCH2OHЃЌдйЗЂЩњДпЛЏбѕЛЏЩњГЩCH2=CHCHOЃЌНјвЛВНбѕЛЏЩњГЩCH2=CHCOOHЃЌзюКѓгыЧтбѕЛЏФЦШмвКЗДгІЕУЕНCH2=CH2COONaЃЌдквЛЖЈЬѕМўЯТЗЂЩњМгОлЗДгІПЩЩњГЩФПБъЮяЃЌКЯГЩТЗЯпСїГЬЭМЮЊЃК ЃЌ
ЃЌ
ЙЪД№АИЮЊЃК ЁЃ
ЁЃ

ЁОЬтФПЁПМзДМЪЧвЛжжПЩдйЩњФмдДЃЌОпгаЙуЗКЕФгІгУЧАОАЁЃЙЄвЕЩЯВЩгУЯТСаСНжжЗДгІКЯГЩМзДМЃК
ЗДгІIЃКCO(g)ЃЋ2H2(g)![]() CH3OH(g) ІЄH1
CH3OH(g) ІЄH1
ЗДгІIIЃКCO2(g)ЃЋ3H2(g)![]() CH3OH(g) + H2O(g) ІЄH2
CH3OH(g) + H2O(g) ІЄH2
ЃЈ1ЃЉЯТБэЫљСаЪ§ОнЪЧЗДгІIдкВЛЭЌЮТЖШЯТЕФЛЏбЇЦНКтГЃЪ§ЃЈKЃЉЁЃ
ЮТЖШ | 250Ёц | 300Ёц | 350Ёц |
K | 2.04 | 0.25 | 0.012 |
ЂйгЩБэжаЪ§ОнХаЖЯІЄH1 _________0 ЃЈЬюЁАЃОЁБЁЂЁАЃНЁБЛђЁАЃМЁБЃЉЁЃ
ЂкФГЮТЖШЯТЃЌНЋ2 mol COКЭ6 mol H2ГфШы2 LЕФУмБеШнЦїжаЃЌ5 minКѓДяЕНЦНКтЃЌВтЕУc(CO)ЃН0.2 molЃЏLЃЌдђгУH2БэЪОЕФ5minФкИУЗДгІЕФЗДгІЫйТЪv(H2)=_______molЁЄL-1ЁЄmin-1ЃЌИУЮТЖШЯТДЫЗДгІЕФЦНКтГЃЪ§ЮЊ___________ЃЌДЫЪБЕФЮТЖШЮЊ________ЃЈДгЩЯБэжабЁдёЃЉЁЃ
ЃЈ2ЃЉвЛЖЈЬѕМўЯТЃЌНЋ1 mol COгы 3 mol H2ЕФЛьКЯЦјЬхдкДпЛЏМСзїгУЯТФмздЗЂЗДгІЩњГЩМзДМЁЃШєШнЦїШнЛ§ВЛБфЃЌЯТСаДыЪЉПЩЬсИпCOзЊЛЏТЪЕФЪЧ________ЁЃ
AЃЎЩ§ИпЮТЖШ BЃЎНЋCH3OHЃЈgЃЉДгЬхЯЕжаЗжРы
CЃЎКуШнЬѕМўЯТГфШыHe DЃЎдйГфШыЪЪСПЕФ H2
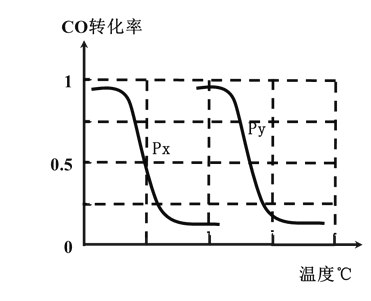
ЃЈ3ЃЉЮЊСЫбАевКЯГЩМзДМЕФЮТЖШКЭбЙЧПЕФЪЪвЫЬѕМўЃЌФГЭЌбЇЩшМЦСЫШ§зщЪЕбщЃЌВПЗжЪЕбщЬѕМўвбОЬюдкЯТУцЪЕбщЩшМЦБэжаЁЃ
ЪЕбщБрКХ | ЮТЖШЃЈЁцЃЉ | n(CO)/n(H2) | бЙЧПЃЈMPaЃЉ |
1 | a | 1/2 | 0.2 |
2 | 200 | b | 5 |
3 | 350 | 1/2 | 0.2 |
AЃЎдђЩЯБэжаЪЃгрЕФЪЕбщЬѕМўЪ§ОнЃКa=________ЁЂb=_______ЁЃ
BЃЎИљОнЗДгІIЕФЬиЕуЃЌзѓЯТЭМЪЧдкбЙЧПЗжБ№ЮЊ0.2MPaКЭ5MPaЯТCOЕФзЊЛЏТЪЫцЮТЖШБфЛЏЕФЧњЯпЭМЃЌЧыжИУїЭМжаЕФбЙЧПPy=______MPaЁЃ
ЃЈ4ЃЉЩЯЪіЗДгІжаашвЊгУЕНH2зіЗДгІЮяЃЌвдМзЭщЮЊдСЯжЦШЁЧтЦјЪЧГЃгУЕФжЦЧтЗНЗЈЁЃвбжЊЃК
ЂйCH4(g) + H2O(g) = CO(g) + 3H2(g) ІЄH = +206.2 kJЁЄmol-1
ЂкCH4(g) + CO2(g) = 2CO(g) + 2H2(g) ІЄH = +247.4 kJЁЄmol-1
дђCH4КЭH2O(g)ЗДгІЩњГЩCO2КЭH2ЕФШШЛЏбЇЗНГЬЪНЮЊЃК__________________________ЁЃ