题目内容
7.设NA是阿伏加德罗常数的数值,下列说法正确的是( )| A. | 7.8g 苯中含有的单键数目为0.9NA | |
| B. | 1 mol Cl2溶于水,与水反应时电子转移数目为1 NA | |
| C. | 在298K 1.01×105pa下,22 g CO2和N2O混合气体中,所占的体积大于11.2升 | |
| D. | 常温下,pH=13的NaOH溶液中含有的OH-离子数目为0.1NA |
分析 A、苯不是单双键交替的结构;
B、氯气和水的反应为可逆反应;
C、CO2和N2O的摩尔质量均为44g/mol;
D、溶液体积不明确.
解答 解:A、苯不是单双键交替的结构,故苯中无碳碳单键,故A错误;
B、氯气和水的反应为可逆反应,不能进行彻底,故转移的电子数小于NA个,故B错误;
C、CO2和N2O的摩尔质量均为44g/mol,故22g混合物的物质的量为0.5mol,而298K 1.01×105pa下,气体摩尔体积大于22.4L/mol,故0.5mol混合气体的体积大于11.2L,故C正确;
D、溶液体积不明确,故溶液中的氢氧根的个数无法计算,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
4.在烧瓶中充满标准状况下干燥的HCl和N2、O2的混合气,已知其平均相对分子质量为34.8,进行喷泉实验后,理论上所得溶液的物质的量浓度为( )
| A. | 0.022mol•L-1 | B. | 0.045mol•L-1 | C. | 0.8mol•L-1 | D. | 无法计算 |
18.化学与生活密切相关,下列说法不正确的是( )
| A. | 二氧化硫可广泛用于食品的增白 | |
| B. | 聚乙烯塑料制品可用于食品的包装 | |
| C. | 次氯酸钠溶液可用于环境的消毒杀菌 | |
| D. | 氧化铝是冶炼金属铝的原料,也是一种较好的耐火材料 |
15.下列实验操作中正确合理的是( )
| A. | 用100 mL容量瓶配制50 mL 0.1 mol/L盐酸 | |
| B. | 在托盘天平上称量NaOH时,应将NaOH固体放在小烧杯中称量 | |
| C. | 用25 mL量筒量取4.0 mol/L的盐酸5.62 mL | |
| D. | 用托盘天平准确称取5.85 g NaCl固体 |
2.下表是元素周期表的一部分,根据表中列出的10种元素,回答下列问题.
(1)非金属性最强的元素是F;
(2)Ne原子结构示意图为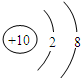 ;
;
(3)N和O中,原子半径较小的是O; (4)H2S和HCl中,热稳定性较强的是HCl;
(5)MgO和Al2O3中,属于两性氧化物的是Al2O3;
(6)元素最高价氧化物对应的水化物中,碱性最强的是NaOH(填化学式);
(7)SiO2常用于制造光导纤维(填一种高性能的现代通讯材料的名称);
(8)誉称为“绿色氧化剂”的过氧化氢,它的化学式是H2O2,其中氢元素与氧元素的质量比为m(H):m(O)=1:16;(相对原子质量:H-1,O-16)
(9)镁是制造汽车、飞机、火箭的重要材料.写出工业上电解熔融氯化镁获得金属镁的化学方程式:MgCl2(熔融)$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2.
| 周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | N | O | F | Ne | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
(2)Ne原子结构示意图为
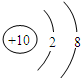 ;
;(3)N和O中,原子半径较小的是O; (4)H2S和HCl中,热稳定性较强的是HCl;
(5)MgO和Al2O3中,属于两性氧化物的是Al2O3;
(6)元素最高价氧化物对应的水化物中,碱性最强的是NaOH(填化学式);
(7)SiO2常用于制造光导纤维(填一种高性能的现代通讯材料的名称);
(8)誉称为“绿色氧化剂”的过氧化氢,它的化学式是H2O2,其中氢元素与氧元素的质量比为m(H):m(O)=1:16;(相对原子质量:H-1,O-16)
(9)镁是制造汽车、飞机、火箭的重要材料.写出工业上电解熔融氯化镁获得金属镁的化学方程式:MgCl2(熔融)$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2.
12.下列说法正确的是( )
| A. | 在100℃、101 kPa条件下,液态水的气化热为40.69 kJ•mol-1,则H2O(g)?H2O(l) 的△H=40.69 kJ•mol-1 | |||||||||||
| B. | 100mL pH=2的新制氯水中:N(OH-)+N(ClO-)+N(HClO)=0.001NA | |||||||||||
| C. | 已知:
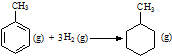 的焓变为△H=[(4×348+3×610+8×413)+3×436-(7×348+14×413)]kJ•mol-1=-384 kJ•mol-1 的焓变为△H=[(4×348+3×610+8×413)+3×436-(7×348+14×413)]kJ•mol-1=-384 kJ•mol-1 | |||||||||||
| D. | 常温下,在0.10 mol•L-1的NH3•H2O溶液中加入少量NH4Cl晶体,能使NH3•H2O的电离度降低,溶液的pH减小 |