题目内容
17.亚氯酸钠(NaClO2)是一种强氧化性漂白剂,它在碱性环境中稳定存在,广泛应用于纺织、印染和食品工业.某同学查阅资料后,设计出一种获得NaClO2的转化流程如图所示.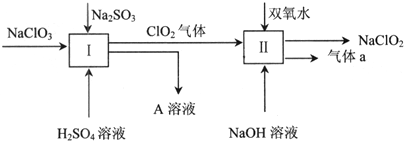
(1)I中发生反应的还原剂是Na2SO3(填化学式).
(2)A溶液中溶质的化学式是Na2SO4.
(3)Ⅱ中反应的离子方程式如下,请补充完整.2ClO2+H2O2+22OH-=2ClO2-+O2↑+2H2O.
分析 由制备流程可知,硫酸钠溶液通I中,NaClO2、Na2SO3发生氧化还原反应,离子反应方程式为2ClO3-+2H++SO32-=2ClO2↑+SO42-+H2O;然后ClO2和双氧水在II中发生氧化还原反应生成NaClO2和气体a,该反应中Cl元素化合价由+4价变为+3价,则O元素化合价由-1价变为0价,所以生成的气体a是O2,以此来解答.
解答 解:由制备流程可知,硫酸钠溶液通I中,NaClO2、Na2SO3发生氧化还原反应,离子反应方程式为2ClO3-+2H++SO32-=2ClO2↑+SO42-+H2O;然后ClO2和双氧水在II中发生氧化还原反应生成NaClO2和气体a,该反应中Cl元素化合价由+4价变为+3价,则O元素化合价由-1价变为0价,所以生成的气体a是O2,
(1)I中发生2ClO3-+2H++SO32-=2ClO2↑+SO42-+H2O,S元素的化合价升高,则还原剂为Na2SO3,故答案为:Na2SO3;
(2)由I中反应可知,反应后为硫酸钠溶液,溶质为Na2SO4,故答案为:Na2SO4;
(3)Cl元素的化合价降低,O元素的化合价应升高,该反应生成氧气,且反应在碱性溶液中进行,则由电子、电荷守恒可知,离子反应为2ClO2+H2O2+2OH-=2ClO2-+O2↑+2H2O,故答案为:2OH-;O2↑.
点评 本题考查制备实验,为高频考点,把握物质的性质、制备流程中的反应为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案
相关题目
7.设NA是阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 7.8g 苯中含有的单键数目为0.9NA | |
| B. | 1 mol Cl2溶于水,与水反应时电子转移数目为1 NA | |
| C. | 在298K 1.01×105pa下,22 g CO2和N2O混合气体中,所占的体积大于11.2升 | |
| D. | 常温下,pH=13的NaOH溶液中含有的OH-离子数目为0.1NA |
8.X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如表:
(1)Y的元素符号是SS.
(2)XY2是一种常用的溶剂,XY2的分子中存在2个σ键.在H-Y、H-Z两种共价键中,键的极性较强的是H-Cl,键长较长的是H-S.
(3)W的基态原子核外电子排布式是1s22s22p63s23p63d104s1.
(4)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y.此反应的化学方程式是2CO+SO2=S+2CO2.
(5)请设计一个实验方案,比较Y、Z单质氧化性的强弱:在Na2S溶液中滴加Cl2水,若溶液出现浑浊,说明Cl2的氧化性比S强.
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
(2)XY2是一种常用的溶剂,XY2的分子中存在2个σ键.在H-Y、H-Z两种共价键中,键的极性较强的是H-Cl,键长较长的是H-S.
(3)W的基态原子核外电子排布式是1s22s22p63s23p63d104s1.
(4)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y.此反应的化学方程式是2CO+SO2=S+2CO2.
(5)请设计一个实验方案,比较Y、Z单质氧化性的强弱:在Na2S溶液中滴加Cl2水,若溶液出现浑浊,说明Cl2的氧化性比S强.
5.下列各组物质中,因为反应条件或用量不同而发生不同化学反应的是( )
①C与O2 ②Na与O2 ③Fe与Cl2
④AlCl3溶液与氨水 ⑤CO2与NaOH溶液 ⑥Cu与硝酸.
①C与O2 ②Na与O2 ③Fe与Cl2
④AlCl3溶液与氨水 ⑤CO2与NaOH溶液 ⑥Cu与硝酸.
| A. | 除③外 | B. | 除④外 | C. | 除③④外 | D. | 除②⑥外 |
2.下列说法正确的是( )
| A. | 丙烯分子中有7个σ键,2个π键 | |
| B. | 在60 g SiO2晶体中,Si-O键的数目为2NA | |
| C. | l mol金刚石中,含2 mol C-C键 | |
| D. | 由ⅠA族和ⅥA族元素形成的原子个数比为1:1,电子总数为38的化合物,是含有共价键的离子化合物 |
9.火箭推进器常以联氨(N2H4) 为燃料、过氧化氢为助燃剂.已知下列各物质反应的热化学方程式:
N2H4(g)+O2(g)=N2(g)+2H2O(g)△H1=-533.23kJ•mol-1
H2O(g)=H2O (l)△H2=-44kJ•mol-1
2H2O2(l)=2H2O(l)+O2(g)△H3=-196.4kJ•mol-1
则联氨与过氧化氢反应的热化学方程式可表示为( )
N2H4(g)+O2(g)=N2(g)+2H2O(g)△H1=-533.23kJ•mol-1
H2O(g)=H2O (l)△H2=-44kJ•mol-1
2H2O2(l)=2H2O(l)+O2(g)△H3=-196.4kJ•mol-1
则联氨与过氧化氢反应的热化学方程式可表示为( )
| A. | N2H4(g)+2H2O2(l)=N2(g)+4H2O(l)△H=+817.63 kJ•mol-1 | |
| B. | N2H4(g)+2H2O2(l)=N2(g)+4H2O(g)△H=-641.63 kJ•mol-1 | |
| C. | N2H4(g)+2H2O2(l)=N2(g)+4H2O(l)△H=-641.63 kJ•mol-1 | |
| D. | N2H4(g)+2H2O2(l)=N2(g)+4H2O(g)△H=-817.63 kJ•mol-1 |
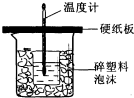 50mL 0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算反应热.请回答下列问题:
50mL 0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算反应热.请回答下列问题: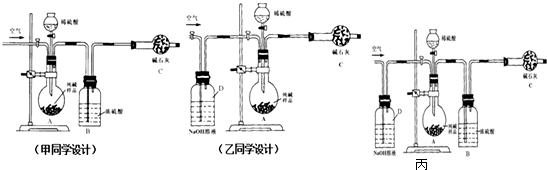
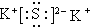 ,CO2的结构式为O=C=O.
,CO2的结构式为O=C=O.