题目内容
【题目】下列有关溶液![]() 室温下
室温下![]() 的说法正确的是
的说法正确的是![]()
A.![]() 和
和![]() 形成的混合溶液中:
形成的混合溶液中:![]()
B.![]() 溶液中通入
溶液中通入![]() 至溶液
至溶液![]() :
:![]()
C.物质的量浓度相等的![]() 溶液、
溶液、![]() 溶液、
溶液、![]() 溶液、
溶液、![]() 溶液中,
溶液中,![]() 的大小关系:
的大小关系:![]()
D.![]() 溶液中通入HCl至溶液
溶液中通入HCl至溶液![]() :
:![]()
【答案】D
【解析】
A.没有指明溶液的浓度和体积,无法判断离子浓度大小,故A错误;
B.溶液中钠离子与S原子物质的量之比为1:1,而铵根离子与部分亚硫酸根结合,故![]() ,由物料守恒可知,
,由物料守恒可知,![]() ,溶液呈中性,由电荷守恒可得:
,溶液呈中性,由电荷守恒可得:![]() ,联立可得:
,联立可得:![]() ,
,![]() ,故B错误;
,故B错误;
C.由于亚铁离子水解抑制铵根离子水解,故![]() ,由于碳酸氢根离子水解促进铵根离子水解,故
,由于碳酸氢根离子水解促进铵根离子水解,故![]() ,故离子浓度大小为:
,故离子浓度大小为:![]() ;故C错误;
;故C错误;
D.![]() 溶液中通入HCl气体至
溶液中通入HCl气体至![]() ,则
,则![]() ,根据电荷守恒可得:
,根据电荷守恒可得:![]() ,则
,则![]() ,结合物料守恒
,结合物料守恒![]() 可知,
可知,![]() ,所以浓度大小为:
,所以浓度大小为:![]() ,故D正确;
,故D正确;
故选D。

【题目】在2 L密闭容器内,800 ℃时反应2NO(g)+O2(g)![]() 2NO2(g) ΔH<0,n(NO)随时间的变化如下表:
2NO2(g) ΔH<0,n(NO)随时间的变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)下图中表示NO2的变化的曲线是_____。用O2表示从0~2 s内该反应的平均速率v=____。

(2)能说明该反应已达到平衡状态的是____。
A.v(NO2)=2v(O2) B.容器内压强保持不变
C.v逆(NO)=2v正(O2) D.容器内密度保持不变
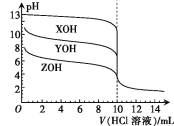
【题目】25℃时,用浓度为0.100 0 mol·L-1的氢氧化钠溶液分别滴定20.00 mL浓度均为0.100 0 mol·L-1的二种酸HX、HY(忽略体积变化),实验数据如下表,下列判断不正确的是 ( )
数据编号 | 滴入NaOH(aq)的体积/mL | 溶液的pH | |
HX | HY | ||
① | 0 | 3 | 1 |
② | a | 7 | x |
③ | 20.00 | >7 | y |
A. 在相同温度下,同浓度的两种酸溶液的导电能力:HX<HY
B. 由表中数据可估算出Ka(HX)≈10-5
C. HY和HX混合,c(H+)=c(X-)+c(Y-)+c(OH-)
D. 上述②反应后的HY溶液中:c(Na+)>c(Y-)>c(OH-)>c(H+)
【题目】下表为元素周期表中第四周期的部分元素![]() 从左到右按原子序数递增排列
从左到右按原子序数递增排列![]() ,根据要求回答下列问题:
,根据要求回答下列问题:
K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge |
(1)以上元素的基态原子的电子排布中,4s轨道上只有1个电子的元素有______![]() 填元素名称
填元素名称![]() 。
。
(2)以上元素中,属于s区的元素有_________种,属于d区的元素有______种。
(3)第一电离能![]() ________
________![]() 填“
填“![]() ”、“
”、“![]() ”或“
”或“![]() ”,下同
”,下同![]() 。
。
(4)现有含钛的两种颜色的晶体,![]() 的配位数均为6,一种为紫色,一种为绿色,相关实验证明,两种晶体的组成皆为
的配位数均为6,一种为紫色,一种为绿色,相关实验证明,两种晶体的组成皆为![]() 。为测定这两种晶体的化学式,设计了如下实验:
。为测定这两种晶体的化学式,设计了如下实验:
![]() 分别取等质量的两种配合物晶体的样品配成待测溶液;
分别取等质量的两种配合物晶体的样品配成待测溶液;
![]() 分别往待测溶液中滴入
分别往待测溶液中滴入![]() 溶液,均产生白色沉淀;
溶液,均产生白色沉淀;
![]() 溶液反应得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的
溶液反应得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的![]() 。试推断紫色晶体的化学式为_________。
。试推断紫色晶体的化学式为_________。
(5)含有元素K的盐的焰色反应为__________色。许多金属盐都可以发生焰色反应,其原因是____________。
(6)立方氮化硼晶体![]() ,是一种超硬材料,有优异的耐磨性,其晶胞如图所示。
,是一种超硬材料,有优异的耐磨性,其晶胞如图所示。
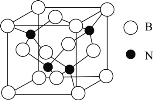
若立方氮化硼晶胞的边长为![]() ,则立方氮化硼的密度为________g/cm3
,则立方氮化硼的密度为________g/cm3![]() 只要求列算式,不必计算出数值,阿伏加德罗常数的值为NA)。
只要求列算式,不必计算出数值,阿伏加德罗常数的值为NA)。