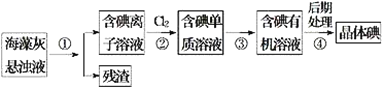
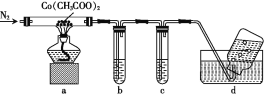
题目内容
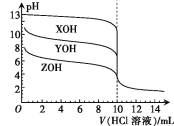
【题目】常温下,XOH、YOH及ZOH三种一元碱的物质的量浓度均为0.100 mol·L-1,体积均为10.00 mL,分别用0.100 mol·L-1的HCl溶液滴定,滴定曲线如图所示。下列说法正确的是
A.均可用酚酞作指示剂
B.电离平衡常数:Kb(YOH)<Kb(ZOH)
C.均滴入10.00 mL HCl溶液时,ZCl溶液中的水解程度最大
D.pH=11的YOH与pH=3的HCl溶液等体积混合:c(Cl-)>c(Y+)>c(H+)>c(OH-)
【答案】C
【解析】
0.1mol/L的XOH溶液pH=13,说明XOH完全电离,为强碱;而YOH、ZOH为弱碱,三者碱性强弱为XOH>YOH>ZOH,都滴入10.00 mL HCl溶液时均恰好完全反应生成正盐,YCl、ZCl要水解,且ZCl水解程度更大。
A、XOH为强碱,YOH、ZOH为弱碱,用盐酸滴定弱碱时应用甲基橙做指示剂,故A错误;
B、有图像看出,YOH、ZOH的物质的量浓度均为0.100 mol·L-1时,YOH溶液的pH更大,则碱性更强,所以电离平衡常数Kb(YOH)>Kb(ZOH),故B错误;
C、均滴入10.00 mL HCl溶液时,YCl、ZCl要水解,而ZOH碱性最弱,所以ZCl水解程度最大,故C正确;
D、YOH时弱碱,pH=11的YOH与pH=3的HCl溶液等体积混合时,YOH过量,溶液应显碱性,离子浓度顺序为:c(Y+) > c(Cl-) > c(OH-) > c(H+),故D错误。
答案选C。

【题目】氯化铁是常见的水处理剂,利用废铁屑可制备无水氯化铁。实验室制备装置和工业制备流程图如下:
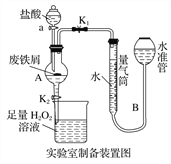
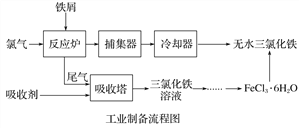
已知:(1)无水FeCl3的熔点为555 K、沸点为588 K。
(2)废铁屑中的杂质不与盐酸反应。
(3)不同温度下六水合氯化铁在水中的溶解度如下:
温度/℃ | 0 | 20 | 80 | 100 |
溶解度(g/100 g H2O) | 74.4 | 91.8 | 525.8 | 535.7 |
实验室制备操作步骤如下:
Ⅰ.打开弹簧夹K1,关闭活塞K2,并打开活塞a,缓慢滴加盐酸;
Ⅱ.当……时,关闭弹簧夹K1,打开活塞K2,当A中溶液完全进入烧杯后关闭活塞a;
Ⅲ.将烧杯中溶液经过一系列操作后得到FeCl3·6H2O晶体。
请回答:
(1)烧杯中足量的H2O2溶液的作用是_____________________________。
(2)为了测定废铁屑中铁的质量分数,操作Ⅱ中“…”的内容是______________。
(3)从FeCl3溶液制得FeCl3·6H2O晶体的操作步骤是加入______________后__________________、过滤、洗涤、干燥。
(4)试写出吸收塔中反应的离子方程式:______________________。
(5)捕集器温度超过673 K时,存在相对分子质量为325的铁的氯化物,该物质的分子式(相对原子质量:Cl-35.5、Fe-56)为____________。
(6)FeCl3的质量分数通常可用碘量法测定:称取m g无水氯化铁样品,溶于稀盐酸,配制成100 mL溶液;取出10.00 mL,加入稍过量的KI溶液,充分反应后,滴入几滴淀粉溶液,并用c mol·L-1 Na2S2O3溶液滴定,消耗V mL(已知:I2+2S2O32-=2I-+S4O62-)。
①滴定终点的现象是________________________________________________;
②样品中氯化铁的质量分数为__________________________。