��Ŀ����
����Ŀ��2017��5��18���й����ʵ�����������ҹ����Ϻ����еĿ�ȼ���Բɻ�óɹ�����Ϊȫ���һ����ÿ�ȼ�������ȶ������Ĺ��ҡ���ȼ������Ȼ����ˮ������γɵľ������ʣ���Ҫ�����ڶ�����ͺ��״�½���С�����˵����ȷ����( )

�ټ����������ࣻ����ͬ�����£�������ܶȴ��ڿ������ܶȣ��ۼ���������ˮ���ܿ�ȼ����һ�ּ���DZ������Դ������ظ�ԭ���ܴ��ھ����������ȼ����
A.�٢ۢܢ�B.�ڢۢܢ�C.�٢ڢۢ�D.�٢ڢܢ�
���𰸡�A
��������
�ټ�������C��HԪ����ɵ������������ȷ��
�ڼ������Է�������Ϊ16����ͬ�����£��ܶȱȿ���С���ڴ���
�ۼ���������ˮ������ȷ��
�ܼ�����ȫȼ�����ɶ�����̼��ˮ��Ϊ�����Դ������ȷ��
������ȼ������ˮ����Ȼ��������γɵľ������ʣ���Ҫ�����ڶ�����ͺ��״�½���У�������ظ�ԭ��������ܴ��ڷḻ������ȼ����������ȷ��
�ʺ���ѡ����A��

 �Ƹ�С״Ԫͬ������������ϵ�д�
�Ƹ�С״Ԫͬ������������ϵ�д�����Ŀ����������(ClNO)���л��ϳ��е���Ҫ�Լ�������NO��Cl2��ͨ�������·�Ӧ�õ�����ѧ����ʽΪ2NO(g)��Cl2(g)![]() 2ClNO(g)��
2ClNO(g)��
(1)���������������ڴ����еĺ������������ʱ�������������ȣ��漰���·�Ӧ���� 2NO2(g)��NaCl(s)![]() NaNO3(s)��ClNO(g) K1����4NO2(g)��2NaCl(s)
NaNO3(s)��ClNO(g) K1����4NO2(g)��2NaCl(s)![]() 2NaNO3(s)��2NO(g)��Cl2(g) K2����2NO(g)��Cl2(g)
2NaNO3(s)��2NO(g)��Cl2(g) K2����2NO(g)��Cl2(g)![]() 2ClNO(g) K3,��K1��K2��K3֮��Ĺ�ϵΪK3=_______________����K1��K2��ʾ����
2ClNO(g) K3,��K1��K2��K3֮��Ĺ�ϵΪK3=_______________����K1��K2��ʾ����
(2)��֪���ֻ�ѧ���ļ����������±������������ȵĽṹΪCl��N==O��
��ѧ�� | N��O | Cl��Cl | Cl��N | N==O |
����/(kJ��mol��1) | 630 | 243 | a | 607 |
��2NO(g)��Cl2(g)![]() 2ClNO(g)�ķ�Ӧ�� ��H��a�Ĺ�ϵΪ ��H = ___kJ��mol��1��
2ClNO(g)�ķ�Ӧ�� ��H��a�Ĺ�ϵΪ ��H = ___kJ��mol��1��
(3)300��ʱ��2NO(g)��Cl2 (g)![]() 2ClNO(g)������Ӧ���ʱ���ʽΪv�� = k��cn (ClNO)��������ʺ�Ũ�ȵĹ�ϵ���±���
2ClNO(g)������Ӧ���ʱ���ʽΪv�� = k��cn (ClNO)��������ʺ�Ũ�ȵĹ�ϵ���±���
��� | c(ClNO)/(mol��L��1) | v/(mol��L��1��s��l) |
�� | 0. 30 | 3. 60��10��9 |
�� | 0. 60 | 1. 44��10��8 |
�� | 0. 90 | 3. 24��10��8 |
n = ___��k = ____��
(4)������Ⱥ����ܱ������г������ʵ���֮��Ϊ2 : 1��NO��Cl2���з�Ӧ2NO(g)��Cl2(g)![]() 2ClNO(g)�����жϷ�Ӧ�Ѵﵽ��ѧƽ��״̬����__�����ţ���
2ClNO(g)�����жϷ�Ӧ�Ѵﵽ��ѧƽ��״̬����__�����ţ���
a�������е�ѹǿ���� b��2v��(NO) = v��(Cl2)c�������ƽ����Է����������ֲ��� d���÷�Ӧƽ�ⳣ�����ֲ���e��NO��Cl2������ȱ��ֲ���
(5)25��ʱ�������Ϊ2 L�Ҵ���ѹ�Ƶĺ����ܱ�������ͨ��0.08 mol NO��0.04 mol Cl2������Ӧ��2NO(g)��Cl2 (g)![]() 2ClNO(g)��H��
2ClNO(g)��H��
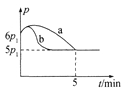
������Ӧ��ʼ��ƽ��ʱ�¶���ͬ����÷�Ӧ������ѹǿ(p)��ʱ��(t)�ı仯��ͼ������a��ʾ���� ��H __���>����<����ȷ������0��������������ͬ�����ı�ijһ����ʱ�������ѹǿ(p)��ʱ��(t)�ı仯��ͼ������b��ʾ����ı��������______��
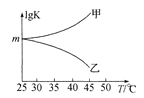
��ͼ�Ǽס���ͬѧ���������Ӧƽ�ⳣ���Ķ���ֵ(lg K)���¶ȵı仯��ϵ��������ȷ��������____����ס����ҡ�����mֵΪ_____��
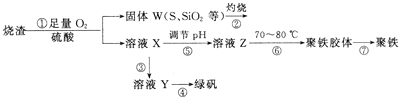
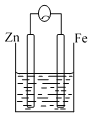
����Ŀ����1�������Ȼ�����Һ�ش��������⣺
����FeCl3��Һ�м�������NaHCO3������������Ϊ___�������ӷ���ʽ��ʾ��ԭ��___��
�ڲ��ϼ���FeCl3��Һ������ˮ�ֲ����գ��õ��Ĺ�����___��
��������FeCl3��Һʱ��Ϊ��ֹ��Һ����ǣ�Ӧ����___��
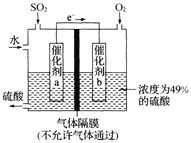
��2�����÷�ӦCu+H2O2+H2SO4=CuSO4+2H2O���һ��ԭ��أ��ش��������⣺
�ٸ�������Ϊ___��������ӦʽΪ___��
�ڷ�Ӧ������SO![]() ��____���ƶ���
��____���ƶ���
�۵���·��ת��0.1mol����ʱ�����Һ����(�����缫)������___�ˡ�
��3����֪25��ʱ����������ʵĵ���ƽ�ⳣ�����������ʾ���ش��������⣺
��ѧʽ | CH3COOH | H2CO3 | HClO |
����ƽ�ⳣ�� | Ka=1.8��10-5 | Ka1=4.3��10-7 Ka2=5.6��10-11 | Ka=3.0��10-8 |
�����ʵ���Ũ�Ⱦ�Ϊ0.1molL-1��������Һ��pH��С�������е�˳����__���ñ����д��
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
�ڳ����£�0.1molL-1CH3COOH��Һ��ˮϡ�����У����б���ʽ�����ݱ�����___������ĸ��
A.c��H+�� B.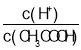 C.c��H+��c��OH-�� D.
C.c��H+��c��OH-�� D.![]() E.
E.![]()
��д�������������Һ��ͨ������������̼�����ӷ���ʽ��____��
��25��ʱ��CH3COOH��CH3COONa�Ļ����Һ������û��ҺpH=6������Һ��c��CH3COO-��-c��Na+��=____����ȷ��ֵ����
�ݱ�״���£���1.12LCO2ͨ��100mL1molL-1��NaOH��Һ�У�����Һ������Ũ�ȷ���������е�ʽ��c��OH-��=2c��H2CO3��+____��