题目内容
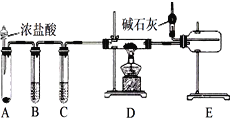
【题目】某化学学习小组利用如图装置来制备无水AlCl3或NaH(已知:AlCl3、NaH遇水都能迅速发生反应)。下列说法错误的是
A. 制备无水AlCl3:装置A中的试剂可能是高锰酸钾
B. 点燃D处酒精灯之前需排尽装置中的空气
C. 装置C中的试剂为浓硫酸
D. 制备无水AlCl3和NaH时球形干燥管中碱石灰的作用完全相同
【答案】D
【解析】
由图可知,装置A为氯气或氢气的制备装置,装置B的目的是除去氯气或氢气中的氯化氢,装置C的目的是干燥氯气或氢气,装置E收集反应生成的氯化铝或氢化钠,碱石灰的作用是防止空气中水蒸气进入E中,或吸收过量的氯气防止污染环境。
A项、浓盐酸可与高锰酸钾常温下发生氧化还原反应制备氯气,故A正确;
B项、因为金属铝或金属钠均能与氧气反应,所以点燃D处酒精灯之前需排尽装置中的空气,故B正确;
C项、装置C中的试剂为浓硫酸,目的是干燥氯气或氢气,故C正确;
D项、制备无水AlCl3时,碱石灰的作用是防止空气中水蒸气进入E中,吸收过量的氯气防止污染环境,制备无水NaH时,碱石灰的作用是防止空气中水蒸气进入E中,故D错误。
故选D。

【题目】PCl3和PCl5都是重要的化工原料。将PCl3(g)和Cl2(g)充入2L的恒容密闭容器中,在一定条件下发生反应PCl3(g)+Cl2(g)![]() PCl5(g),△H<0并于10min时达到平衡。有关数据如下:下列判断正确的是
PCl5(g),△H<0并于10min时达到平衡。有关数据如下:下列判断正确的是
PCl3(g) | Cl2(g) | PCl5(g) | |
初始浓度/(molL-1) | 2.0 | 1.0 | 0 |
平衡浓度/(molL-1) | c1 | c2 | 0.4 |
A.10min内,v(Cl2)=0.02mol/(Lmin)
B.升高温度,反应的平衡常数增大
C.反应达到平衡时容器内的压强与初始时容器的压强之比为1:2
D.平衡后移走2.0molPCl3和1.0molCl2,相同条件下再达平衡时,c(PCl5)<0.2molL-1