题目内容
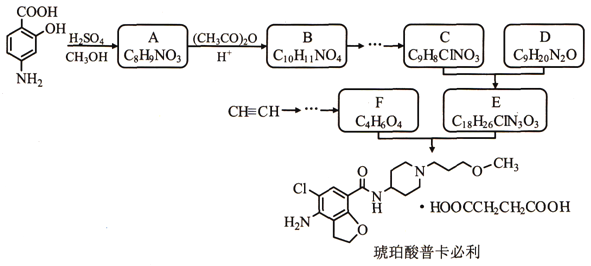
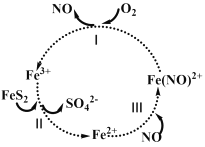
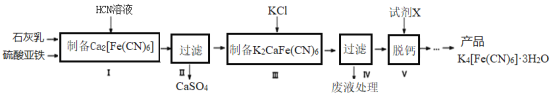
【题目】黄血盐[亚铁氰化钾,K4[Fe(CN)6]目前广泛用做食盐添加剂(抗结剂),我国卫生部规定食盐中黄血盐的最大使用量为10mgkgˉ1。一种制备黄血盐的工艺如下:
回答下列问题:
(1)步骤Ⅰ反应的化学方程式为____________。
(2)步骤Ⅳ过滤所得的废液中含量较多的溶质为(填化学式)___________________。
(3)步骤Ⅴ所用的试剂X是______________________。
【答案】6HCN+3Ca(OH)2+FeSO4=Ca2Fe(CN)6+CaSO4↓+6H2O Ca Cl2(KCl可答) K2CO3
【解析】
本题制备黄血盐的流程先由石灰乳、硫酸亚铁和HCN溶液制得Ca2[Fe(CN)6],过滤除去CaSO4后加入KCl,制得K2Ca[Fe(CN)6],再经过滤除去废液,加入试剂以除去钙并生成K4[Fe(CN)6],再经一系列分离操作获得K4[Fe(CN)6]·3H2O。可在此基础上,解答各小题。
(1)根据流程图,步骤I中投入物质为石灰乳、FeSO4、HCN,生成的物质为Ca2Fe(CN)6,Ca2Fe(CN)6中CN显-1价,Ca显+2价,Fe显+2价,步骤I中没有化合价的变化,因此有Ca(OH)2+FeSO4+HCN→Ca2Fe(CN)6,SO42-与部分Ca2+结合生成微溶的CaSO4形成沉淀,因此反应方程式为 6HCN+3Ca(OH)2+FeSO4=Ca2Fe(CN)6+CaSO4↓+6H2O。答案为: 6HCN+3Ca(OH)2+FeSO4=Ca2Fe(CN)6+CaSO4↓+6H2O;
(2)根据步骤III,加入KCl制备K2CaFe(CN)6,2个K+替代了一个Ca2+,滤液中含有的溶质为CaCl2,以及过量的KCl;答案为:CaCl2(KCl可答);
(3)根据流程目的,同时为了不引入新的杂质,应加入含K+的物质,步骤V是脱钙,试剂X中应含有能与Ca2+结合的阴离子,因此加入试剂X应为K2CO3;答案为:K2CO3

【题目】催化还原CO2是解决温室效应及能源问题的重要手段之一。研究表明,在Cu/ZnO催化剂存在下,在CO2中通入H2,二者可发生以下两个平行反应:
反应Ⅰ CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH1=-53.7 kJ·mol-1
CH3OH(g)+H2O(g) ΔH1=-53.7 kJ·mol-1
反应Ⅱ CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH2=+41.2 kJ·mol-1
CO(g)+H2O(g) ΔH2=+41.2 kJ·mol-1
(1)反应Ⅰ的化学平衡常数表达式是K=_______________________________。
(2)一定温度下,在容积可变的密闭容器中进行反应Ⅱ,不能确定上述可逆反应已达到化学平衡状态的是_____________
A.体系的体积不再发生变化 B.生成n mol CO的同时消耗n mol H2O
C.混合气的密度不再改变 D.1 mol H—H键断裂的同时断裂2 mol H—O键
(3)某实验室控制一定的CO2和H2初始投料比,在相同压强下,经过相同的反应时间测得如下实验数据(其中“甲醇选择性”是指转化的CO2中生成甲醇的百分比):
反应序号 | T/K | 催化剂 | CO2转化率/% | 甲醇选择性/% |
① | 543 | Cu/ZnO纳米棒 | 12.3 | 42.3 |
② | 543 | Cu/ZnO纳米片 | 10.9 | 72.7 |
③ | 553 | Cu/ZnO纳米棒 | 15.3 | 39.1 |
④ | 553 | Cu/ZnO纳米片 | 12.0 | 71.6 |
①对比表中①和③可发现:同样催化剂条件下,温度升高,CO2转化率升高, 而甲醇的选择性却降低,请解释甲醇选择性降低的可能原因________________________________;
②对比表中①、②可发现,在同样温度下,采用Cu/ZnO纳米片使CO2转化率降低, 而甲醇的选择性却提高,请解释甲醇的选择性提高的可能原因___________________________________________。
③有利于提高CO2转化为CH3OH平衡转化率的措施有____________。
a.使用Cu/ZnO纳米棒做催化剂 b.使用Cu/ZnO纳米片做催化剂
c.降低反应温度 d.投料比不变,增加反应物的浓度
e.增大CO2和H2的初始投料比
(4)反应混合气体经过降温加压可分离出甲醇,剩余气体可再次充入反应器继续反应,经过多次循环往复后混合气体中CO的含量已经很高,可以在另外容器中在合适的催化剂条件下使CO和H2反应合成CH3OH(g),写出该反应的热化学方程式:_______________________________。