题目内容
【题目】S2Cl2是一种金黄色易挥发的液体,常用作橡胶硫化剂。某化学兴趣小组拟设计 实验制备少量的S2Cl2,査阅资料知:
①干燥的氯气在 110℃~140℃与硫反应,即可得到 S2Cl2。
②S 的熔点为 112.8℃、沸点为 444.6℃;S2Cl2 的熔点为-76℃、沸点为 138℃。
③S2Cl2+Cl2![]() 2SCl2。
2SCl2。
④S2Cl2 易和水发生歧化反应。

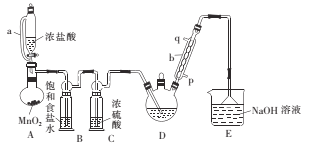
该小组设计的制备装置如如图(夹持仪器和加热装置已略去)
(1)连接好实验装置后的第一步实验操作是____________。
(2)A 装置中制取氯气的离子反应方程式_____________。
(3)装置 B、C 中的试剂分别是_____________,_____________; 若实验中缺少 C 装置,发现产品浑浊不清,请用化学方程式表示其原因____________。
(4)该实验的操作顺序应为_____________(用序号表示)。
①加热装置 A ②加热装置 D ③通冷凝水 ④停止加热装置 A ⑤停止加热装置 D
(5)图中 G 装置中应放置的试剂为______________,其作用为______________。
(6)在加热 D 时温度不宜过高,其原因是_______________; 为了提高 S2Cl2 的纯度,关键的操作是控制好温度和______________。
【答案】检查装置的气密性 MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O 饱和食盐水 浓硫酸 2S2C12+2H2O=3S↓+SO2↑+4HCl ①③②⑤④或者③①②⑤④ 碱石灰 吸收氯气尾气,防止空气中的水蒸气进入装置使S2Cl2水解 产品纯度降低 控制盐酸的滴速不要过快
Mn2++Cl2↑+2H2O 饱和食盐水 浓硫酸 2S2C12+2H2O=3S↓+SO2↑+4HCl ①③②⑤④或者③①②⑤④ 碱石灰 吸收氯气尾气,防止空气中的水蒸气进入装置使S2Cl2水解 产品纯度降低 控制盐酸的滴速不要过快
【解析】
装置A、B、C是制取干燥纯净的氯气,所以B是除杂装置,C是干燥装置;制得产品S2Cl2易水解,所以该装置前后均需要干燥环境,可推出装置G作用;实验操作顺序按照合理、安全原则进行;最后按照题干已知条件进行答题,据此分析。
(1)连接好装置后需检查装置的气密性,答案为:检查装置的气密性;
(2)MnO2与浓盐酸反应的离子方程式为:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
(3)B是除去氯气中的HCl,用饱和食盐水溶液;C是干燥装置,用浓硫酸;若缺少干燥装置,则产物S2Cl2与水发生歧化反应且变浑浊,2S2Cl2+2H2O=3S↓+SO2↑+4HCl;答案为:饱和食盐水;浓硫酸;2S2Cl2+2H2O=3S↓+SO2↑+4HCl;
(4)加热之前先通冷凝水,否则开始生成的S2Cl2不能冷却液化,最后先停止加热后再停止通氯气,平衡容器压强,实验操作为:①③②⑤④或者③①②⑤④;
(5)G装置在最后一步,其作用之一未反应完的氯气尾气处理,其二防止空气中的水蒸气进入装置,G中盛放碱石灰,作用是吸收氯气尾气,防止空气污染,且防止空气中的水蒸气进入装置使S2Cl2水解;
(6)根据已知条件,温度太高S会汽化进入F装置,导致产率降低;为了提高 S2Cl2 的纯度,关键的操作除了控制好温度外,还可以控制盐酸的滴速不要过快。

 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案【题目】某化学兴趣小组为研究过氧化钠与SO2的反应情况,进行如下探究。
(1)[提出假设]
向一定量的过氧化钠固体中通入足量的SO2,对反应后的固体产物成分及反应原理提出如下假设:
假设一:反应后固体中只有Na2SO3,证明SO2未被氧化;
假设二:反应后固体中只有Na2SO4,证明SO2完全被氧化;
假设三:反应后固体______,证明SO2部分被氧化。
(2)[定性研究]
为验证假设三,该小组进行如下研究,请你完成下表中内容。
实验步骤(不要求写出具体操作过程) | 预期的实验现象和结论 |
取适量反应后的固体放入试管中,____ | ______ |
(3)[定量研究]
通过测量气体的体积判断发生的化学反应,实验装置如图:
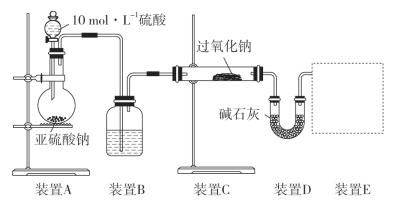
①装置B中所盛装试剂的名称为________。
②装置D的作用是__________。
③请画出实验装置E_____。
④实验测得装置C中过氧化钠质量增加了m1 g,装置D质量增加了m2 g,装置E中收集到的气体为V L(已换算成标准状况下),用上述有关测量数据进行填表判断。
SO2被氧化的程度 | V与m1或m2的关系 |
未被氧化 | |
完全被氧化 | V=0 |
部分被氧化 | _____ |