题目内容
下列各组离子一定能在指定溶液中大量共存的是( )
①无色溶液中:K+、OH-、SO42-、HC2O4-
②使pH试纸变深蓝色的溶液中:Na+、CO32-、S2-、SO32-
③水电离的c(H+)=1×10-12mol?L-1的溶液中:Al3+、ClO-、HCO3-、SO42-
④加入Mg能放出H2的溶液中:Mg2+、NH4+、Cl-、SO4-
⑤使石蕊变红的溶液中:Na+、Fe2+、SO42-、MnO4-
⑥pH=0的溶液中:Fe3+、NO3-、Cl-、I-.
①无色溶液中:K+、OH-、SO42-、HC2O4-
②使pH试纸变深蓝色的溶液中:Na+、CO32-、S2-、SO32-
③水电离的c(H+)=1×10-12mol?L-1的溶液中:Al3+、ClO-、HCO3-、SO42-
④加入Mg能放出H2的溶液中:Mg2+、NH4+、Cl-、SO4-
⑤使石蕊变红的溶液中:Na+、Fe2+、SO42-、MnO4-
⑥pH=0的溶液中:Fe3+、NO3-、Cl-、I-.
| A、①③ | B、②④ | C、①⑤ | D、③⑥ |
考点:离子共存问题
专题:离子反应专题
分析:①无色溶液中不存在有色离子,草酸氢根离子与氢氧根离子发生反应;
②使pH试纸变深蓝色的溶液为碱性溶液,Na+、CO32-、S2-、SO32-之间不发生反应,也不与氢氧根离子反应;
③水电离的c(H+)=1×10-12mol?L-1的溶液为 酸性或者碱性溶液,碳酸氢根离子能够与铝离子、氢离子、氢氧根离子反应、铝离子能够与氢氧根离子反应、次氯酸根离子能够与氢离子反应;
④加入Mg能放出H2的溶液为酸性溶液,Mg2+、NH4+、Cl-、SO4-离子之间不发生反应,也不与氢离子反应;
⑤使石蕊变红的溶液为酸性溶液,酸性条件下高锰酸根离子能够氧化亚铁离子;
⑥pH=0的溶液为酸性溶液,硝酸根离子在酸性条件下能够氧化碘离子、铁离子能够氧化碘离子.
②使pH试纸变深蓝色的溶液为碱性溶液,Na+、CO32-、S2-、SO32-之间不发生反应,也不与氢氧根离子反应;
③水电离的c(H+)=1×10-12mol?L-1的溶液为 酸性或者碱性溶液,碳酸氢根离子能够与铝离子、氢离子、氢氧根离子反应、铝离子能够与氢氧根离子反应、次氯酸根离子能够与氢离子反应;
④加入Mg能放出H2的溶液为酸性溶液,Mg2+、NH4+、Cl-、SO4-离子之间不发生反应,也不与氢离子反应;
⑤使石蕊变红的溶液为酸性溶液,酸性条件下高锰酸根离子能够氧化亚铁离子;
⑥pH=0的溶液为酸性溶液,硝酸根离子在酸性条件下能够氧化碘离子、铁离子能够氧化碘离子.
解答:
解:①无色溶液中,OH-与HC2O4-发生中和反应,在溶液中不能大量共存,故①错误;
②使pH试纸变深蓝色的溶液中存在大量的氢氧根离子,Na+、CO32-、S2-、SO32-之间不发生反应,且都不与氢氧根离子反应,在溶液中能够大量共存,故②正确;
③水电离的c(H+)=1×10-12mol?L-1的溶液为酸性或者碱性溶液,Al3+与OH-、HCO3-发生反应ClO-、HCO3-与氢离子反应,在溶液中不能大量共存,故③错误;
④加入Mg能放出H2的溶液中存在大量的氢离子,Mg2+、NH4+、Cl-、SO4-之间不反应,且都不与氢离子反应,在溶液中能够大量共存,故④正确;
⑤使石蕊变红的溶液为酸性溶液,酸性条件下MnO4-能够氧化Fe2+,在溶液中不能大量共存,故⑤错误;
⑥pH=0的溶液中中存在大量氢离子,硝酸根离子在酸性条件下具有强氧化性,Fe3+、NO3-能够氧化I-,在溶液中不能大量共存,故⑥错误;
故选B.
②使pH试纸变深蓝色的溶液中存在大量的氢氧根离子,Na+、CO32-、S2-、SO32-之间不发生反应,且都不与氢氧根离子反应,在溶液中能够大量共存,故②正确;
③水电离的c(H+)=1×10-12mol?L-1的溶液为酸性或者碱性溶液,Al3+与OH-、HCO3-发生反应ClO-、HCO3-与氢离子反应,在溶液中不能大量共存,故③错误;
④加入Mg能放出H2的溶液中存在大量的氢离子,Mg2+、NH4+、Cl-、SO4-之间不反应,且都不与氢离子反应,在溶液中能够大量共存,故④正确;
⑤使石蕊变红的溶液为酸性溶液,酸性条件下MnO4-能够氧化Fe2+,在溶液中不能大量共存,故⑤错误;
⑥pH=0的溶液中中存在大量氢离子,硝酸根离子在酸性条件下具有强氧化性,Fe3+、NO3-能够氧化I-,在溶液中不能大量共存,故⑥错误;
故选B.
点评:本题考查离子共存的正误判断,为高考中的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间;能生成难溶物的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
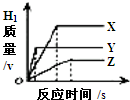 将相同体积、相同溶质质量分教的稀盐酸,分别加入到等质量、颗粒大小相同的X、Y、Z三种较活泼金属中(金属完全反应〕,生成H2的质量与反应时间的关系如图所示.下列说法中正确的是( )
将相同体积、相同溶质质量分教的稀盐酸,分别加入到等质量、颗粒大小相同的X、Y、Z三种较活泼金属中(金属完全反应〕,生成H2的质量与反应时间的关系如图所示.下列说法中正确的是( )| A、三种金属的活动性顺序为Y>X>Z |
| B、产生氢气的速率顺序为X>Y>Z |
| C、消耗稀盐酸的质量顺序为Z>Y>X |
| D、相对原子质量由大到小的顺序为X>Y>Z |
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A、常温下,18g H2O中含H2数目为NA |
| B、标准状况下,22.4L H2O中含有化学键的数目为2NA |
| C、将0.5mol SO2通入足量水中,充分反应后可得到H2 SO3分子数为0.5NA |
| D、常温常压下,Na2O2与足量H2O反应,共生成0.2mol O2,转移电子的数目为0.4NA |
下列与有机物的结构、性质有关的叙述正确的是( )
| A、乙烯和聚乙烯都可以与溴水发生加成反应 |
| B、醇与所有酸的反应都是酯化反应 |
| C、乙烷与氯气发生取代反应生成的有机物共有9种 |
| D、在有机物分子中,两个羟基去掉一分子水的反应就是酯化反应 |
下列指定物质的个数比不为1:1的是( )
| A、D2O中质子数与中子数 |
| B、Na2O2中的阴,阳离子数 |
| C、SO2与氯水反应生成两种强酸的反应中,氧化剂与还原剂 |
| D、沸水时纯水中H+与OH- |
下列属于化学性质的是 ( )
| A、溶解性 | B、挥发性 |
| C、金属活动性 | D、导电性 |
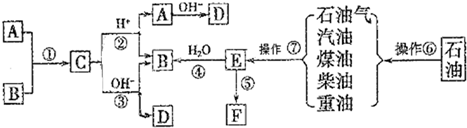
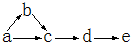 a、b、c、d、e是含有一种相同元素的五种物质,可发生如右图所示的转化.其中:a是单质;c、d是氧化物;e是最高价氧化物对应的水化物.
a、b、c、d、e是含有一种相同元素的五种物质,可发生如右图所示的转化.其中:a是单质;c、d是氧化物;e是最高价氧化物对应的水化物.