题目内容
3.氯水中存在如下平衡:Cl2(g)?Cl2(aq)、Cl2(aq)+H2O?H++Cl-+HClO.下列说法正确的是( )| A. | 向饱和氯水中通入HCl,有c(H+)═c(Cl-)+c(OH-)+c(ClO-) | |
| B. | 氯气在1mol•L-1的NaCl溶液中比在1mol•L-1的AlCl3溶液中的溶解度小 | |
| C. | 光照,氯水的漂白性增强 | |
| D. | 若向饱和氯水中通入少量H2S,则$\frac{c({H}^{+})}{c(ClO^-)}$减小 |
分析 A、溶液中电荷守恒分析判断;
B、氯化铝溶液中氯离子浓度大,对化学平衡抑制程度大;
C、光照次氯酸分解为盐酸和氧气,漂白性是次氯酸的性质;
D、次氯酸具有氧化性氧化硫化氢,消耗ClO-,氢离子浓度增大.
解答 解:A、溶液中电荷守恒分析,向饱和氯水中通入HCl,有电荷守恒为:c(H+)=c(Cl-)+c(OH-)+c(ClO-),故A正确;
B、氯化铝溶液中氯离子浓度大,对化学平衡抑制程度大,氯气在1mol•L-1的NaCl溶液中比在1mol•L-1的AlCl3溶液中的溶解度大,故B错误;
C、光照次氯酸分解为盐酸和氧气,漂白性是次氯酸的性质,漂白性减弱,故C错误;
D、次氯酸具有氧化性氧化硫化氢,消耗ClO-,氢离子浓度增大,则$\frac{c({H}^{+})}{c(ClO^-)}$增大,故D错误;
故选A.
点评 本题考查了化学平衡影响因素,弱电解质电离,物质性质的理解应用,掌握基础是解题关键,题目难度中等.

练习册系列答案
相关题目
13.下列说法正确的是( )
| A. | SiH4比CH4稳定 | |
| B. | O2- 半径比F- 的小 | |
| C. | Na和Cs属于第ⅠA族元素,Cs失电子能力比Na的强 | |
| D. | P和S属于第三周期的元素,H3PO4酸性比H2SO4的弱 |
14.下列过程发生了物理变化的是( )
| A. | 碘的萃取 | B. | 电解食盐水 | C. | 葡萄酿酒 | D. | 金属冶炼 |
11.下列说法正确的是( )
| A. | △H<0、△S>0的反应在温度低时不能自发进行 | |
| B. | 在其他外界条件不变的情况下,使用催化剂可改变化学反应进行的方向 | |
| C. | 因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应自发性的判据 | |
| D. | NH4HCO3(s)═NH3 (g)+H2O(g)+CO2 (g)△H=+185.57 kJ/mol可能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 |
8.下列物质的转变,不能一步实现的( )
| A. | Al2O3→Al(OH)3 | B. | KNO3→KOH | C. | Zn→ZnCl2 | D. | MgCl2→Mg(OH)2 |
6.某化学小组以苯甲酸为原料制取苯甲酸甲酯.有关物质的沸点和相对分子质量如表:
Ⅰ.合成苯甲酸甲酯粗产品
在烧瓶中加入12.2g苯甲酸和20mL甲醇(密度约0.79g/mL),再小心加入3mL浓硫酸,混匀后,投入几粒碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品.
(1)该反应中浓硫酸的作用,若反应产物水分子中有同位素18O,写出能表示反应前后18O位置的化学方程式:C6H5CO18OH+CH3OH催化剂加热$?_{△}^{催化剂}$H5COOCH3+H218O,甲醇过量的原因该反应是可逆反应,甲醇比苯甲酸价廉,且甲醇沸点低,易损失,增加甲醇的量,可提高产率.
(2)如果加热一段时间后发现忘记加碎瓷片,应该采取的正确操作是冷却后补加.
(3)甲、乙、丙三位同学分别设计了如图1三套实验室制取苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去).根据有机物的特点,最好采用装置乙(填“甲”、“乙”、“丙”).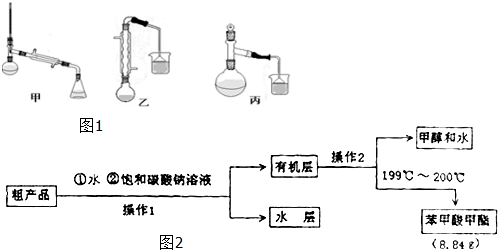
Ⅱ.粗产品的精制
(4)苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,现拟用图2流程图进行精制,请根据流程图填入恰当操作方法的名称:操作I为,操作Ⅱ为分液,蒸馏.
(5)如图2流程图中加入Na2CO3溶液后,放入分液漏斗中振荡、静置,要得到有机层,其具体操作是将分液漏斗上口的玻璃塞打开(或使塞上的凹槽对准漏斗口上的小孔),再旋开分液漏斗活塞,用锥形瓶接收下层液体,待下层液体刚好流尽时关闭活塞,将有机层从分液漏斗上口倒入另一干净的容器(或烧杯)中.
(6)苯甲酸甲酯的产率为65%.
Ⅰ.合成苯甲酸甲酯粗产品
| 物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
| 沸点/℃ | 64.7 | 249 | 199.6 |
| 相对分子质量 | 32 | 122 | 136 |
(1)该反应中浓硫酸的作用,若反应产物水分子中有同位素18O,写出能表示反应前后18O位置的化学方程式:C6H5CO18OH+CH3OH催化剂加热$?_{△}^{催化剂}$H5COOCH3+H218O,甲醇过量的原因该反应是可逆反应,甲醇比苯甲酸价廉,且甲醇沸点低,易损失,增加甲醇的量,可提高产率.
(2)如果加热一段时间后发现忘记加碎瓷片,应该采取的正确操作是冷却后补加.
(3)甲、乙、丙三位同学分别设计了如图1三套实验室制取苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去).根据有机物的特点,最好采用装置乙(填“甲”、“乙”、“丙”).

Ⅱ.粗产品的精制
(4)苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,现拟用图2流程图进行精制,请根据流程图填入恰当操作方法的名称:操作I为,操作Ⅱ为分液,蒸馏.
(5)如图2流程图中加入Na2CO3溶液后,放入分液漏斗中振荡、静置,要得到有机层,其具体操作是将分液漏斗上口的玻璃塞打开(或使塞上的凹槽对准漏斗口上的小孔),再旋开分液漏斗活塞,用锥形瓶接收下层液体,待下层液体刚好流尽时关闭活塞,将有机层从分液漏斗上口倒入另一干净的容器(或烧杯)中.
(6)苯甲酸甲酯的产率为65%.
3.下列命名正确的是( )
| A. | 1、2-二甲基丁烷 | B. | 4-乙基戊烷 | ||
| C. | 3-甲基己烷 | D. | 2,3-二甲基-3-丁烯 |
 已知1-丙醇和2-丙醇的结构简式如下:
已知1-丙醇和2-丙醇的结构简式如下: