题目内容
5.如图是Cu-Zn原电池的装置示意图,下列叙述正确的是( )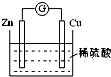
| A. | Zn片是正极 | B. | H+在铜片上得电子 | ||
| C. | 反应过程中电能转变为化学能 | D. | 电子从锌片通过硫酸溶液流向铜片 |
分析 Cu-Zn-稀硫酸原电池放电时,化学能转变为电能,较活泼的金属锌作负极,较不活泼的金属铜作正极,负极上失电子发生氧化反应,正极上得电子发生还原反应,电子从负极沿导线流向正极,据此分析.
解答 解:A、Cu-Zn-稀硫酸原电池放电时,较活泼的金属锌作负极,负极上失电子发生氧化反应,故A错误;
B、较不活泼的金属铜作正极,正极H+在铜片上得电子发生还原反应,故B正确;
C、该原电池放电时,化学能转变为电能,故C错误;
D、电子从负极锌片沿导线流向正极铜片,不经过溶液,故D错误.
故选B.
点评 本题考查了原电池原理,难度不大,注意把握正负极的判断方法,难点是判断电子从负极锌片沿导线流向正极铜片,不经过溶液.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案
相关题目
15.设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | NA个氧气分子与NA个氖气分子的质量比是4:5 | |
| B. | 17gOH-与19gH3O+所含质子数相等 | |
| C. | 标准状况下,11.2LCO2与常温常压下8.5gNH3所含分子数相等 | |
| D. | 12g C和16g O所含的原子数不相等 |
16.下列说法正确的是( )
| A. | 过量的100gNa2O2与CO2反应后,固体质量变成了105.6g,此反应转移电子为0.4mol | |
| B. | 在Fe与含nmolHNO3的稀溶液反应中,被还原的HNO3不一定为$\frac{1}{4}$nmol | |
| C. | 在Mg与Al做电极,其它溶液做电解质构成原电池中,Mg一定为负极 | |
| D. | 碱性氧化物一定为金属氧化物,酸性氧化物不一定是非金属氧化物 |
13.电池对环境的污染目前还没有被人们充分的认识到,下列有关电池污染及回收的有关叙述正确的是( )
| A. | 电池一般比较小,即使埋到土壤中也不会造成太大危害 | |
| B. | 电池回收的主要目的是为了提取里面的银、汞等金属 | |
| C. | 废旧电池可以直接通过燃烧的方式销毁 | |
| D. | 电池不仅污染土壤,也污染地下水 |
20.目前地球环境污染问题越来越严重,已成为世界各国普遍关注和研究的问题.请分析并回答下列问题:
(1)如表数据是济南市2014年6月15日的空气质量日报:
请从表中选出:①首要污染物是可吸入颗粒物;
②能引起光化学烟雾的是二氧化硫、二氧化氮(从表中选).
(2)在一些工业发达国家的城市都相继发生过光化学烟雾事件,并造成数以千计的人员伤亡,光化学烟雾事件产生的主要原因是AD.
A.汽油的不完全燃烧 B.大量使用了化肥和农药
C.白色塑料垃圾的漂浮 D.汽车尾气的排放
(3)酸雨给人类带来种种危害,严重威胁着生态环境.①称为酸雨的水溶液的pH范围是B.
A.pH<7 B.pH<5.6 C.pH>5.6 D.pH<0
②请举一例说明酸雨的危害腐蚀建筑物、使土壤、水等酸化、腐蚀农作物等.
③我国是燃煤大国,采用石灰石-石膏法进行烟道气脱硫,请写出工业脱硫并制取石膏的化学方程式CaCO3+SO2=CaSO3+CO2,2CaSO3+O2=2CaSO4.
(1)如表数据是济南市2014年6月15日的空气质量日报:
| 污染指数 | 首要污染物 | 空气质量级别 | 空气 质量状况 | ||
| 二氧化硫 | 二氧化氮 | 可吸入颗粒物 | |||
| 12 | 33 | 68 | 2 | 良 | |
②能引起光化学烟雾的是二氧化硫、二氧化氮(从表中选).
(2)在一些工业发达国家的城市都相继发生过光化学烟雾事件,并造成数以千计的人员伤亡,光化学烟雾事件产生的主要原因是AD.
A.汽油的不完全燃烧 B.大量使用了化肥和农药
C.白色塑料垃圾的漂浮 D.汽车尾气的排放
(3)酸雨给人类带来种种危害,严重威胁着生态环境.①称为酸雨的水溶液的pH范围是B.
A.pH<7 B.pH<5.6 C.pH>5.6 D.pH<0
②请举一例说明酸雨的危害腐蚀建筑物、使土壤、水等酸化、腐蚀农作物等.
③我国是燃煤大国,采用石灰石-石膏法进行烟道气脱硫,请写出工业脱硫并制取石膏的化学方程式CaCO3+SO2=CaSO3+CO2,2CaSO3+O2=2CaSO4.
 A、B、C、D、E五种元素是周期表中前四周期的元素.只有A、B、C为金属且同周期,原子序数A<B<C.A、C核外均没有未成对电子;B原子核外有二个未成对电子和三个空轨道.D原子最外层电子数是其周期序数的三倍.E能与D形成化合物ED2,可用于自来水的消毒.
A、B、C、D、E五种元素是周期表中前四周期的元素.只有A、B、C为金属且同周期,原子序数A<B<C.A、C核外均没有未成对电子;B原子核外有二个未成对电子和三个空轨道.D原子最外层电子数是其周期序数的三倍.E能与D形成化合物ED2,可用于自来水的消毒.
 、④HCHO,其中碳原子采取sp2杂化的分子有①③④(填物质序号),HCHO分子的立体结构为平面三角形;
、④HCHO,其中碳原子采取sp2杂化的分子有①③④(填物质序号),HCHO分子的立体结构为平面三角形;