��Ŀ����
16��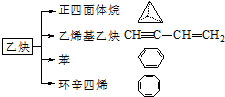 ��Ȳ��һ����Ҫ���л�����ԭ�ϣ�����ȲΪԭ���ڲ�ͬ�ķ�Ӧ�����¿���ת�������»����
��Ȳ��һ����Ҫ���л�����ԭ�ϣ�����ȲΪԭ���ڲ�ͬ�ķ�Ӧ�����¿���ת�������»����������и��⣺
��1������������ķ���ʽΪC4H4�������ȡ��������1�֣�
��2��������ϩ����Ȳ���ӵ�˵��������ǣ�d
a����ʹ����KMnO4��Һ��ɫ
b��1mol��ϩ����Ȳ����3mol Br2�����ӳɷ�Ӧ
c����ϩ����Ȳ�����ں������ֹ�����
d������������Ȳ����ϩ����Ȳ��ȫȼ��ʱ�ĺ���������ͬ
��3��д���뻷����ϩ��Ϊͬ���칹�������ڷ������ķ��ӵĽṹ��ʽ��
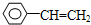 ��
����4��д���뱽��Ϊͬϵ����һ�ȴ���ֻ�����ֵ����ʵĽṹ��ʽ
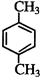 ��
��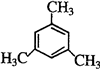 ��
����5������ȲΪ��Ҫԭ�ϣ���ѡ��Ҫ�����Լ����ϳɾ�����ϩ
 ����д���йػ�ѧ��Ӧ����ʽ��CH��CH+HCl$��_{��}^{����}$CH2=CHCl��nCH2=CHCl$\stackrel{һ������}{��}$
����д���йػ�ѧ��Ӧ����ʽ��CH��CH+HCl$��_{��}^{����}$CH2=CHCl��nCH2=CHCl$\stackrel{һ������}{��}$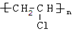 ��
��
���� ��1������������̼ԭ�ӵijɼ���ʽ�ж�̼ԭ�Ӻ���ԭ�ӵĸ������������������в�ͬ�����µ���ԭ�ӵ������ж϶��ȴ����������
��2����ϩ����Ȳ�к���̼̼˫����̼̼����������ϩ����Ȳ�����ʣ�
��3��������ϩ�ķ���ʽΪC8H8�������Ͷ�Ϊ5�����ڷ�������ͬ���칹�壬����1�����������������Ͷ�Ϊ1���ʺ���1������Ϊ-CH=CH2��
��4��һ�ȴ���ֻ�����ֱ���ͬϵ��ڽṹ��Ӧ���нϺõĶԳ��ԣ��ȴ�ʱ������ȡ�������ϵ��⣬Ҳ����ȡ�������ϵ��⣬�Բ���Ϊ�����
��5����Ȳ���Ȼ��ⷢ���ӳɷ�Ӧ��Ȼ�����Ӿ۷�Ӧ��
��� �⣺��1�����������������ÿ���������һ��̼ԭ�ӣ�̼���γ�4�Թ��õ��Ӷԣ�ÿ��̼ԭ���϶�����һ����ԭ�ӣ�����������ķ���ʽΪC4H4��
�������������Ϊ��������Գƽṹ��������ֻ��1��Hԭ�ӣ��������ȴ�����ֻ��1�֣�
�ʴ�Ϊ��C4H4��1��
��2��a���÷����к���̼̼˫����̼̼����������ϩ����Ȳ�����ʣ������ܱ�����KMnO4��Һ������ʹ���Ը��������Һ��ɫ������ȷ��
b��̼̼˫����̼̼�������ܺ��巢���ӳɷ�Ӧ��1mol̼̼˫����ȫ�ӳ���Ҫ1mol�壬1mol̼̼������ȫ�ӳ���Ҫ2mol�壬����1mol��ϩ����Ȳ����3mol Br2�����ӳɷ�Ӧ������ȷ��
c���÷����к���̼̼˫����������������ϩ����Ȳ�����ں������ֹ����ţ�����ȷ��
d����Ȳ����ϩȲ�����ʽ��ͬ�����Ե���������Ȳ����ϩ����Ȳ��ȫȼ��ʱ�ĺ�������ͬ���ʴ���
��ѡd��
��3��������ϩ�ķ���ʽΪC8H8�������Ͷ�Ϊ5�����ڷ�������ͬ���칹�壬����1�����������������Ͷ�Ϊ1���ʺ���1������Ϊ-CH=CH2�����ڷ�������ͬ���칹��Ľṹ��ʽΪ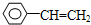 ���ʴ�Ϊ��
���ʴ�Ϊ��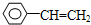 ��
��
��4���뱽��Ϊͬϵ�����Ϊ�����һ�ȴ���ֻ�����֣�˵�����л�����ֻ��2��Hԭ�ӣ��뱽��Ϊͬϵ����һ�ȴ������������ʣ����뿼�ǶԳƽṹ���������ȡ����-CH3������������������ʵĽṹ��ʽΪ�� ��
�� �ȣ��ʴ�Ϊ��
�ȣ��ʴ�Ϊ�� ��
�� ��
��
��5����Ȳ���Ȼ��ⷢ���ӳɷ�Ӧ��Ȼ�����Ӿ۷�Ӧ��CH��CH+HCl$��_{��}^{����}$CH2=CHCl��nCH2=CHCl$\stackrel{һ������}{��}$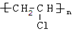 ���ʴ�Ϊ��CH��CH+HCl$��_{��}^{����}$CH2=CHCl��nCH2=CHCl$\stackrel{һ������}{��}$
���ʴ�Ϊ��CH��CH+HCl$��_{��}^{����}$CH2=CHCl��nCH2=CHCl$\stackrel{һ������}{��}$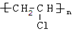 ��
��
���� ���⿼���л���Ľṹ�����ʡ�ͬ���칹�����д�Լ���ѧ����ʽ����д���Ѷ��еȣ��Ƕ��л���ѧ֪ʶ���ۺ����ã���Ϥ�����л���Ľṹ�������ǽ���Ĺؼ���

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д� 2013��9�£��й��������е������������ص������������������ӱ������ϵȵصĿ�����Ⱦ��Ϊ6��������Ⱦ�������ض���Ⱦ������β����ȼú����������ȡů�ŷŵ�C02�ȶ��������γɵ�ԭ��
2013��9�£��й��������е������������ص������������������ӱ������ϵȵصĿ�����Ⱦ��Ϊ6��������Ⱦ�������ض���Ⱦ������β����ȼú����������ȡů�ŷŵ�C02�ȶ��������γɵ�ԭ����1������β����������Ҫԭ��Ϊ��2N0��g��+2C0��g��$\stackrel{����}{?}$N2��g��+2C02��g����H��0����һ���¶��£���һ����̶����ܱ������г���һ������NO��CO��t1ʱ�̴ﵽƽ��״̬��
�����жϸ÷�Ӧ�ﵽƽ��״̬�ı�־��CD��
A���ڵ�λʱ��������1mol CO2��ͬʱ������lmol CO
B�����������ܶȲ��ٸı�
C����������ƽ����Է����������ٸı�
D����������ѹǿ���ٱ仯
����t2ʱ�̣����������ݻ�Ѹ������ԭ����2�����������������������£�t3ʱ�̴ﵽ�µ�ƽ��״̬��֮���ٸı�����������ͼ�в��仭����t2��t4ʱ������Ӧ������ʱ��ı仯���ߣ�
����Ҫͬʱ��߸÷�Ӧ�����ʺ�NO��ת���ʣ���ȡ�Ĵ�ʩ������ѹǿ���������г���CO���壮��д��2����
��2���ı�ú�����÷�ʽ�ɼ��ٻ�����Ⱦ��ͨ���ɽ�ˮ����ͨ�����ȵ�̼�õ�ˮú�����䷴Ӧ��
C��s��+H2O��g��?CO��g��+H2��g����H=+131.3•mol-1
�ٸ÷�Ӧ�ڸ��������Է����У�����¡����£�������
��ú���������в������к�����H2S����������Na2C03��Һ���գ��÷�Ӧ�����ӷ���ʽΪCO32-+H2S=HCO3-+HS-������֪��H2S��Ka1�T9.1��10-18��Ka2�T1.1��10-12��H2CO3��Ka1�T4.3��10-7��Ka2�T5.6��10-11����
��3����֪��Ӧ��CO��g��+H20��g��?CO2��g��+H2��g�����ֽ���ͬ����CO��g����H20��g���ֱ�ͨ�˵����Ϊ2L�ĺ����ܱ������н��з�Ӧ���õ������������ݣ�
| ʵ���� | �¶� �� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
��ʵ��3�У���ƽ��ʱ��CO��ת���ʴ���ˮ��������a��b��������Ĺ�ϵ��a��b��
�۸÷�Ӧ�ġ�H��0�������������������9000Cʱ������һ��ʵ�飬�ڴ������м���l0mol C0��5mo1H20��2mo1C02��5mol H2�����ʱV����V���������������������=������
| A�� | �������ռ���Һ�����ӷ���ʽ��Al+2OH-�TAlO2-+H2�� | |
| B�� | пͭԭ���������Ӧʽ��Cu-2e-�TCu2+ | |
| C�� | ������ĵ��뷽��ʽ��HClO?H++ClO- | |
| D�� | ��֪�к���Ϊ57.3 kJ•mol-1��ϡ��������������ϡ��Һ��Ӧ���Ȼ�ѧ����ʽΪ��H2SO4 ��aq��+2NaOH ��aq���TNa2SO4 ��aq��+2H2O �� l ����H=-57.3 kJ•mol-1 |
| A�� | HOCH2CH2OH | B�� | HOCH2CH��OH��CH3 | C�� | HOCH2CH2CH2OH | D�� | CH3CH��OH��CH��OH��CH3 |
| A�� | ��SiO2������ˮ����SiO2�������������� | |
| B�� | �ڷ�ӦSiO2+2C$\frac{\underline{\;����\;}}{\;}$Si+2CO����SiO2�������� | |
| C�� | SiO2��һ�ֿռ�������״�ṹ�ľ��壬�۵�ߡ�Ӳ�ȴ� | |
| D�� | ������ܹ���ʴ�������ʲ����ò���ƿ��ʢװ����� |
| A�� | 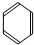 | B�� | 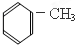 | C�� | 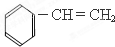 | D�� | 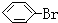 |
| ���� | Fe��OH��2 | Cu��OH��2 | Fe��OH��3 |
| Ksp/25�� | 8.0��10-16 | 2.2��10-20 | 4.0��10-38 |
| ��ȫ����ʱ��pH��Χ | ��9.6 | ��6.4 | 3��4 |
| A�� | ��û����Һ����μ���NaOH��Һ�����ȿ������ɫ���� | |
| B�� | ����Һ��c��SO42-����[c��Cu2+��+c��Fe2+��+c��Fe3+��]��5��4 | |
| C�� | �����Һ�м���������ˮ��������pH��3��4����ˣ��ɻ�ô�����CuSO4��Һ | |
| D�� | ��pH=5����Һ��Fe3+���ܴ������� |
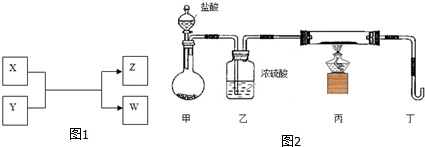
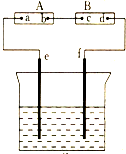 ͼ��AΪ��Դ��BΪ������ʳ��ˮ�ͷ�̪��Һ����ֽ��CΪʢ��ϡ����ĵ��ۣ�e��fΪ���缫����ͨ��·����B�ϵ�c��Ϊ��ɫ���Իش�
ͼ��AΪ��Դ��BΪ������ʳ��ˮ�ͷ�̪��Һ����ֽ��CΪʢ��ϡ����ĵ��ۣ�e��fΪ���缫����ͨ��·����B�ϵ�c��Ϊ��ɫ���Իش�