题目内容
11.有机物甲能发生银镜反应,甲催化加氢还原成有机物乙,1mol乙跟足量的金属钠反应放出标准状况下氢气22.4L,据此推断乙一定不是( )| A. | HOCH2CH2OH | B. | HOCH2CH(OH)CH3 | C. | HOCH2CH2CH2OH | D. | CH3CH(OH)CH(OH)CH3 |
分析 有机物甲能发生银镜反应,含有-CHO,为醛或甲酸形成的酯,甲催化加氢还原成有机物乙,则甲中含有不饱和键,1mol乙跟足量的金属钠反应放出标准状况下H222.4L,氢气的物质的量为1mol,说明乙中含有2个羟基或2个羧基或1个羟基、1个羧基,结合选项判断乙的可能结构,以此解答该题.
解答 解:A.甲为OHCCHO或HOCH2CHO,能发生银镜反应,能与氢气发生加成反应,生成乙为HOCH2CH2OH,1molHOCH2CH2OH与钠反应生成1mol氢气,故A不选;
B.若乙为HOCH2CH(OH)CH3,1mol乙与钠反应生成1mol氢气,甲与氢气发生加成反应生成乙,则甲可以为OHCCH(OH)CH3能发生银镜反应,故B不选;
C.若乙为HOCH2CH2CH2OH,1mol乙与钠反应生成1mol氢气,甲与氢气发生加成反应生成乙,则甲可以为OHCCH2CHO,故C不选;
D.若乙为CH3CH(OH)CH(OH)CH3,1mol乙与钠反应生成1mol氢气,甲与氢气发生加成反应生成乙,则甲不可能含有-CHO,甲不能发生银镜反应,故D选.
故选D.
点评 本题考查有机物的推断,难度中等,掌握官能团的性质与转化是关键,注意利用验证法进行解答.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
19.在一定量的偏铝酸钠溶液中,加入下列哪一种溶液可使获得的沉淀量最大( )
| A. | 硫酸铝 | B. | 盐酸 | C. | 二氧化碳 | D. | 硫酸 |
6.下列说法正确的是( )
| A. | 第ⅠA族元素是同周期中金属性最强的金属元素 | |
| B. | 两个非金属原子间不可能形成离子键 | |
| C. | HF、HCl、HBr和HI的热稳定性和还原性依次减弱 | |
| D. | 根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7 |
3.下列说法正确的是( )
| A. | 碱金属单质的熔点、沸点随着原子序数的递增而逐渐降低 | |
| B. | 过渡元素可用于制备半导体材料 | |
| C. | 碱金属单质的密度随着原子序数的递增而逐渐增大 | |
| D. | 含有离子键的化合物一定是离子化合物 |
11.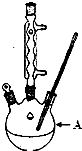 苯甲酸广泛应用于制药和化工行业,某兴趣小组同学利用高锰酸钾氧化甲苯制备苯甲酸
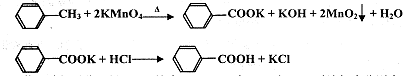
苯甲酸广泛应用于制药和化工行业,某兴趣小组同学利用高锰酸钾氧化甲苯制备苯甲酸
(KMnO4中性条件下还原产物为MnO2,酸性条件下为Mn2+)
已知:苯甲酸相对分子量122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3g和6.9g.
实验流程:
①往装置A中加入2.7mL(2.3g)甲苯和125mL水,然后分批次加入8.5g稍过量的KMnO4固体,控制反应温度约在100℃,当甲苯层近乎消失,回流不再出现油珠时,停止加热.
②将反应混合物趁热过滤,用少量热水洗涤滤渣,合并滤液与洗涤液,冷却后加入浓盐酸,经操作I得白色较干燥粗产品.
③纯度测定:称取1.220g白色样品,配成100mL苯甲酸溶液,取25.00mL溶液,用0.1000mol/L KOH标准溶液滴定,重复滴定四次,每次消耗的体积如表所示.
请回答:
(1)装置A的名称三颈烧瓶.若不用温度计,本实验控制反应温度的措施为沸水浴加热.
(2)白色粗产品中除了KCl外,其他可能的无机杂质为MnCl2.
(3)操作②中趁热过滤的目的是防止苯甲酸结晶析出,减少其损失,操作I的名称过滤、干燥.
(4)步骤③中用到的定量仪器有分析天平,100mL容量瓶,50mL酸式、碱式滴定管.
(5)样品中苯甲酸纯度为96.00%.
(6)滴定操作中,如果对装有KOH标准溶液的滴定管读数时,滴定前仰视,滴定后俯视则测定结果将偏小(填“偏大”、“偏小”或“不变”).
 苯甲酸广泛应用于制药和化工行业,某兴趣小组同学利用高锰酸钾氧化甲苯制备苯甲酸
苯甲酸广泛应用于制药和化工行业,某兴趣小组同学利用高锰酸钾氧化甲苯制备苯甲酸(KMnO4中性条件下还原产物为MnO2,酸性条件下为Mn2+)

已知:苯甲酸相对分子量122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3g和6.9g.
实验流程:
①往装置A中加入2.7mL(2.3g)甲苯和125mL水,然后分批次加入8.5g稍过量的KMnO4固体,控制反应温度约在100℃,当甲苯层近乎消失,回流不再出现油珠时,停止加热.
②将反应混合物趁热过滤,用少量热水洗涤滤渣,合并滤液与洗涤液,冷却后加入浓盐酸,经操作I得白色较干燥粗产品.
③纯度测定:称取1.220g白色样品,配成100mL苯甲酸溶液,取25.00mL溶液,用0.1000mol/L KOH标准溶液滴定,重复滴定四次,每次消耗的体积如表所示.
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 体积(mL) | 24.00 | 24.10 | 22.40 | 23.90 |
(1)装置A的名称三颈烧瓶.若不用温度计,本实验控制反应温度的措施为沸水浴加热.
(2)白色粗产品中除了KCl外,其他可能的无机杂质为MnCl2.
(3)操作②中趁热过滤的目的是防止苯甲酸结晶析出,减少其损失,操作I的名称过滤、干燥.
(4)步骤③中用到的定量仪器有分析天平,100mL容量瓶,50mL酸式、碱式滴定管.
(5)样品中苯甲酸纯度为96.00%.
(6)滴定操作中,如果对装有KOH标准溶液的滴定管读数时,滴定前仰视,滴定后俯视则测定结果将偏小(填“偏大”、“偏小”或“不变”).
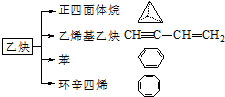 乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.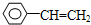 .
.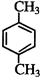 、
、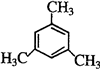 .
. ,试写出有关化学反应方程式:CH≡CH+HCl$→_{△}^{催化剂}$CH2=CHCl,nCH2=CHCl$\stackrel{一定条件}{→}$
,试写出有关化学反应方程式:CH≡CH+HCl$→_{△}^{催化剂}$CH2=CHCl,nCH2=CHCl$\stackrel{一定条件}{→}$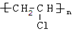 .
.