题目内容
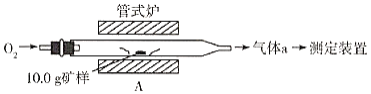
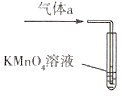
【题目】硒(Se)是第四周期第ⅥA族元素,是人体内不可或缺的微量元素,H2Se是制备新型光伏太阳能电池、半导体材料和金属硒化物的重要原料。
(1)已知:①2H2Se(g)+O2(g)![]() 2Se(s)+2H2O(l) ΔH1=akJ·mol-1
2Se(s)+2H2O(l) ΔH1=akJ·mol-1
②2H2(g)+O2(g)![]() 2H2O(l) ΔH2=bkJ·mol-1
2H2O(l) ΔH2=bkJ·mol-1
反应H2(g)+Se(s)![]() H2Se(g)的ΔH3=__kJ·mol-1(用含a、b的代数式表示)。
H2Se(g)的ΔH3=__kJ·mol-1(用含a、b的代数式表示)。
(2)T℃时,向一恒容密闭容器中加入3molH2和1molSe,发生反应H2(g)+Se(s)![]() H2Se(g)。
H2Se(g)。
①下列情况可判断反应达到平衡状态的是__(填字母代号)。
a.气体的密度不变 b.v(H2)=v(H2Se)
c.气体的压强不变 d.气体的平均摩尔质量不变
②当反应达到平衡后,将平衡混合气体通入气体液化分离器使H2Se气体转化为H2Se液体,并将分离出的H2再次通入发生反应的密闭容器中继续与Se反应时,Se的转化率会提高。请用化学平衡理论解释:_。
③以5小时内得到的H2Se为产量指标,且温度、压强对H2Se产率的影响如图1、图2所示:
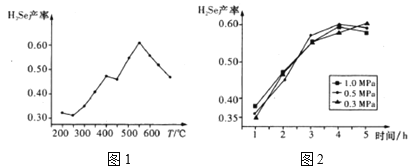
则制备H2Se的最佳温度和压强为__。
(3)已知常温下H2Se的电离平衡常数K1=1.3×10-4、K2=5.0×10-11,则NaHSe溶液呈__(填“酸性”或“碱性”),请通过计算数据说明__。
【答案】![]() (b-a) ad (移除产物H2Se后)将分离出的H2重新通入容器中,平衡正向移动,Se的转化率提高 550℃,0.3MPa 碱性 HSe-的电离常数为K2=5.0×10-11,HSe-的水解常数为7.7×10-11,故电离小于水解,溶液呈碱性
(b-a) ad (移除产物H2Se后)将分离出的H2重新通入容器中,平衡正向移动,Se的转化率提高 550℃,0.3MPa 碱性 HSe-的电离常数为K2=5.0×10-11,HSe-的水解常数为7.7×10-11,故电离小于水解,溶液呈碱性
【解析】
(1)给两个热化学方程式,求目标方程式的反应热,用盖斯定律计算;
(2)①当v(正)=v(逆),体系中各种成分的量不在改变时,达到平衡状态;
②H2Se气体浓度减小、氢气浓度增大,平衡正向移动;
(3)酸式盐的酸碱性,根据Ka×Kh=Kw计算Kh,比较Kh和Ka大小。
![]() 已知①2H2Se(g)+O2(g)
已知①2H2Se(g)+O2(g)![]() 2Se(s)+2H2O(l) ΔH1=akJ·mol-1
2Se(s)+2H2O(l) ΔH1=akJ·mol-1
②2H2(g)+O2(g)![]() 2H2O(l) ΔH2=bkJ·mol-1,
2H2O(l) ΔH2=bkJ·mol-1,
根据盖斯定律,![]() ,可得
,可得![]() 的反应热
的反应热![]()
![]() kJ/mol,故答案为:
kJ/mol,故答案为:![]() ;
;
(2)①a.由于体积不变,有固体参与反应,气体质量在变,故气体的密度不变可作为判定依据,a正确;
![]() 未指明方向,不能作为判定依据,b错误;
未指明方向,不能作为判定依据,b错误;
![]() 此反应为气体体积不变的反应,故气体的压强不变不能作为判定依据,c错误;
此反应为气体体积不变的反应,故气体的压强不变不能作为判定依据,c错误;
![]() 气体的质量改变,气体的物质的量不变,气体的平均摩尔质量不变可作为判定依据,d正确;
气体的质量改变,气体的物质的量不变,气体的平均摩尔质量不变可作为判定依据,d正确;
故答案为:ad;
![]() 将分离出的
将分离出的![]() 重新通入容器中,平衡正向移动,Se的转化率提高,故答案为:(移除产物H2Se后)将分离出的H2重新通入容器中,平衡正向移动,Se的转化率提高;
重新通入容器中,平衡正向移动,Se的转化率提高,故答案为:(移除产物H2Se后)将分离出的H2重新通入容器中,平衡正向移动,Se的转化率提高;
![]() 根据图1和图2知550
根据图1和图2知550![]() ,0.3MPa时产率最高,故答案为:550
,0.3MPa时产率最高,故答案为:550![]() ,0.3MPa;
,0.3MPa;
![]() 由于常温下
由于常温下![]() 的电离平衡常数
的电离平衡常数![]() ,
,![]() ,根据Ka×Kh=Kw得:HSe-的水解常数Kh(HSe-)=
,根据Ka×Kh=Kw得:HSe-的水解常数Kh(HSe-)=![]() =
=![]() ,所以Kh(HSe-)﹥Ka(HSe-),故NaHSe溶液呈碱性,故答案为:碱性;HSe-的电离常数为K2=5.0×10-11,HSe-的水解常数为7.7×10-11,故电离小于水解,溶液呈碱性。
,所以Kh(HSe-)﹥Ka(HSe-),故NaHSe溶液呈碱性,故答案为:碱性;HSe-的电离常数为K2=5.0×10-11,HSe-的水解常数为7.7×10-11,故电离小于水解,溶液呈碱性。

 名校课堂系列答案
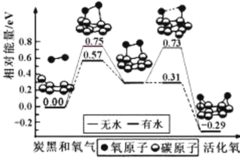
名校课堂系列答案【题目】钛酸钡粉体是电子陶瓷元器件的重要基础原料。工业上以TiCl4、BaCO3、H2C2O4等物质为原料制备草酸氧钛钡晶体[BaTiO(C2O4)2·4H2O],再高温煅烧制得钛酸钡粉体。请回答下列问题:
(1)基态Ti原子的价电子排布图为__,同周期元素中,基态原子未成对电子数与Ti相同的元素有___(填元素符号)。
(2)第IIA族(碱土金属)元素的原子序数、原子半径、第一电离势(从元素的气态基态原子中将一个电子移至无穷远处时所需做的功)如下表所示。
元素 | 原子序数 | 原子半径/pm | 每一电离势/eV |
Be | 4 | 89 | 9.32 |
Mg | 12 | 136 | 7.644 |
Ca | 20 | 174 | 6.111 |
Sr | 38 | 191 | 5.692 |
Ba | 56 | 198 | 5.21 |
①由上表数据可知,相邻元素原子半径差值r(Be-Mg)、r(Mg-Ca)明显大于r(Ca-Sr)、r(Sr-Ba),试解释其原因__。
②由上表数据可知,随原子序数的递增,第IIA族元素的第一电离势依次减小,试解释其原因__。
(3)已知草酸分子的结构简式为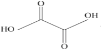 。
。
①草酸分子中,碳原子的杂化方式为__。
②由此结构简式可预测草酸__(填“难溶”“微溶”或“易溶”)于水和乙醇。
③已知草酸和液溴的相关数据如下,草酸熔点高于液溴的原因是__。
名称 | 化学式 | 相对子质量 | 熔点 |
草酸 | H2C2O4 | 90 | 101℃ |
液溴 | Br2 | 160 | -7.2℃ |
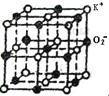
(4)设NA是阿伏加德罗常数的值,已知钛酸钡的立方晶胞结构如图所示,晶胞中Ti原子的配位数为__,其晶胞参数约为apm,钛酸钡晶体的密度ρ=__g.cm-3。(列式即可)