题目内容
【题目】元素性质呈现周期性变化的根本原因是
A. 原子半径呈周期性变化
B. 元素化合价呈周期性变化
C. 电子层数逐渐增加
D. 元素原子的核外电子排布呈周期性变化
【答案】D
【解析】
选D。元素性质呈现周期性变化的根本原因是原子的核外电子排布呈周期性变化。

【题目】(1)已知CH3OH(l)的燃烧热ΔH=-238.6 kJ/mol,CH3OH(l)+3/2O2(g)===CO2(g)+2H2O(g)ΔH=-a kJ/mol,则 a___238.6(填“>”、“<”或“=”)。
(2)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:_________________________________。
(3)反应mA(g)+nB(g)![]() pC(g) +qD(g)过程中的能量变化如图所示,回答下列问题。
pC(g) +qD(g)过程中的能量变化如图所示,回答下列问题。
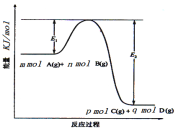
该反应△H =____(用含E1、E2式子表示);在反应体系中加入催化剂,E1___,E2___,(填增大、减小、不变)。
(4)已知:CO (g) +H2O (g)![]() H2 (g) +CO2 (g)平衡常数K随温度的变化如下表:
H2 (g) +CO2 (g)平衡常数K随温度的变化如下表:
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | 1 |
回答下列问题:
①该反应的ΔH=__________填“>”、“=”或“<”)。
②已知在一定温度下,C(s) +CO2 (g)![]() 2CO(g)平衡常数K1;C (s) +H2O (g)
2CO(g)平衡常数K1;C (s) +H2O (g)![]() CO(g) +H2 (g)平衡常数K2。则K、K1 、K2之间的关系是__________________________。
CO(g) +H2 (g)平衡常数K2。则K、K1 、K2之间的关系是__________________________。
【题目】下面是元素周期表的一部分,请按要求填空:
A | B | C | |||||||||||||||
D | E | F | G | ||||||||||||||
H | I | ||||||||||||||||
(1)A元素的最高价氧化物的电子式______。
(2)元素G在周期表中的位置是_______。
(3)C与D简单离子中半径较大的是________(用离子符号表示)。
(4)C与F的气态氢化物中较稳定是________(用化学式表示)。
(5)写出G单质与I的最高价氧化物对应水化物的溶液反应的化学方程式______。
(6)下列说法或实验不能证明H和I两种元素的金属性强弱的是_____。
a 比较两种元素的单质的熔点、沸点高低
b 将两种元素的单质分别与冷水反应,观察反应的剧烈程度
c 比较两种元素的最高价氧化物对应的水化物的碱性强弱