题目内容
【题目】为了探究化学反应的热效应,某兴趣小组进行了如下实验:
(1)将物质X分别装入有水的锥形瓶里,立即塞紧带U形管的塞子,发现U形管内滴有红墨水的水面呈形如图所示状态。

①若如图一所示。该反应是______(填“放热”或“吸热”)反应,X是______(填两种化学式)。
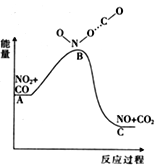
②若如图二所示。该反应是______(填“放热”或“吸热”),以下选项中与其能量变化相同的有______。
A.CO还原CuO的反应 B.CaCO3的分解反应 C.Al和Fe2O3的反应
(2)如图所示,把试管放入盛有25℃饱和石灰水的烧杯中,试管中开始放入几小块铝片,再滴入5 mL稀NaOH溶液。
试回答下列问题:
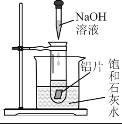
①实验中观察到的现象是:铝片逐渐溶解、铝片上有大量气泡产生、______。
②产生上述现象的原因是______。
【答案】放热 Na或Na2O或CaO(填两种即可) 吸热 B 饱和石灰水中出现白色浑浊 铝和NaOH溶液反应生成H2的反应是放热的,Ca(OH)2的溶解度随温度的升高而降低
【解析】
在探究化学反应的热效应时,如图所示将物质X分别装入有水的锥形瓶里,塞紧带U形管的塞子后,锥形瓶中封闭了一段气体。锥形瓶中的反应吸放热会对封闭气体的体积产生影响,从而使U形管内的红墨水呈形不同状态。如红墨水左低右高,则说明锥形瓶内气体体积膨胀,反应放出热量,该反应为一放热反应。如红墨水左高右低,则说明锥形瓶内气体体积缩小,反应吸收热量,该反应为一吸热反应。据此解题。
(1)
①若如图一所示,体系内气体压力大于外界大气压,说明体系内气体膨胀,反应放热。遇水放热的X物质可以是Na、Na2O、CaO等;
②若如图二所示,体系内气体压力小于外界大气压,说明体系内气体缩小,反应吸热。
A.CO还原CuO的反应为放热反应;
B.CaCO3的分解反应为吸热反应;
C.Al和Fe2O3的反应为放热反应;
故与图示反应能量变化相同的反应应选B;
(2)
①把试管放入盛有25℃饱和石灰水的烧杯中,向试管中开始放入几小块铝片,再滴入5 mL稀NaOH溶液,观察到的现象是:铝片逐渐溶解、铝片上有大量气泡产生、试管外的饱和石灰水中出现白色浑浊。
②产生上述现象的原因是铝和NaOH溶液反应生成H2的反应是放热的,Ca(OH)2的溶解度随温度的升高而降低,因此当温度升高时,有氢氧化钙析出。

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案【题目】Fe是日常生活中最常用的金属之一。回答下列问题:
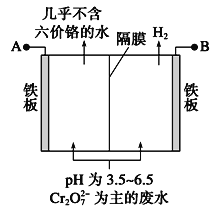
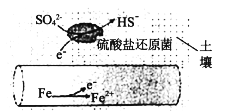
(1)深埋在潮湿土壤中的铁管道,在硫酸盐还原菌(该还原菌最佳生存环境在pH为7~8之间)作用下,能被SO42-腐蚀,其电化学腐蚀原理如下图所示,写出正极的电极反应式___________________。
(2)在1800K时,2Fe(s)+3/2O2(g)=Fe2O3(s) H=-354.2kJ/mol;3Fe(s)+2O2(g)=Fe3O4(s) H=-550.9kJ/mol则反应:2Fe3O4(s)+1/2O2(g) ===3Fe2O3(s)的H为_____ kJ·mol1,四氧化三铁在充满氧气的集气瓶中反应生成Fe2O3_____(填“能”或“不能”)自发进行。
(3)Fe3+和I-在水溶液中的反应如下:2I-+2Fe3+![]() 2Fe2+ +I2(在水溶液中)。
2Fe2+ +I2(在水溶液中)。
①298K时,向5mL 0.1molL1 的KI溶液中滴加0.1molL1 FeCl3溶液,得到c(Fe2+)与加入FeCl3 溶液体积关系如下图所示:

该温度下滴加5mL FeCl3溶液时,Fe3+的平衡转化率=_____%,平衡常数K=_____,若要提高Fe3+的转化率,可采取的措施是________________________。
②在已经达到平衡的上述反应体系中,加入苯对I2进行萃取,保持温度不变,反应速率_____ (填“增大”、“减小”或“不变”),此时υ(正)_____υ(逆)(填“大于”、“小于”或“等于”)。
③υ(正)与Fe3+、I的浓度关系为υ=kc(I-)mc(Fe3+)n(k为常数)
c(I)molL1 | c(Fe3+)molL1 | υ (molL1s1 ) | |
(1) | 0.20 | 0.80 | 0.032k |
(2) | 0.60 | 0.40 | 0.144k |
(3) | 0.80 | 0.20 | 0.128k |
通过分析所给数据计算可知:在υ=kc(I-)mc(Fe3+)n 中,m,n的值为_____(填字母代号)。
A.m=1,n=1 B.m=2,n=1 C.m=2,n=2 D.m=1,n=2