题目内容
4.关于化学键的下列叙述中,正确的是( )| A. | 离子化合物中可能含共价键 | B. | 共价化合物中可能含离子键 | ||
| C. | 离子化合物中不含共价键 | D. | 共价化合物中不含离子键 |
分析 含有离子键的化合物为离子化合物,离子化合物中可能含有共价键,只含共价键的化合物属于共价化合物,共价化合物中一定不含离子键,据此分析解答.
解答 解:A.离子化合物中一定含有离子键,可能含有共价键,如KOH,故A错误;
B.只含共价键的化合物属于共价化合物,共价化合物中一定不含离子键,故B错误;
C.离子化合物中可能含有共价键,如铵盐等,故C错误;
D.只含共价键的化合物属于共价化合物,共价化合物中一定不含离子键,故D正确;
故选D.
点评 本题考查化学键和化合物的关系,侧重考查基本概念,明确物质构成微粒及微粒之间作用力是解本题关键,注意不能根据是否含有金属元素判断化合物类型.

练习册系列答案
相关题目
14.下列有关化学反应原理的说法不正确的是( )
| A. | 强酸和强碱的中和反应的活化能接近于零,所以反应速率很高 | |
| B. | 过程的自发性既能用于判断过程的方向,也能用于判断过程发生的速率 | |
| C. | 电解质溶液导电的过程中,一定发生了电解质溶液的电解 | |
| D. | 溶解度较小的BaSO4在一定条件下也可以转化为溶解度略大的BaCO3 |
15.下列说法错误的是( )
| A. | C2H6和C4H10一定是同系物 | |
| B. | C2H4和C4H8一定是同系物 | |
| C. | 相对分子质量相等的两种物质,不一定是同分异构体 | |
| D. | 烯烃各同系物含碳的质量分数相等 |
9.X、Y、Z、R分别代表四种元素,若aXm+、bYn+、cZn-、dRm-四种离子的核外电子排布相同,且m>n,则下列关系正确的是( )
| A. | a-c=m-n | B. | b+d=m+n | C. | a>b>d>c | D. | a>b>c>d |
13.有两种气态饱和烃的混合物0.1mol,完全燃烧可得标况下6.72L二氧化碳和0.3mol水,这两种烃可能是( )
| A. | C2H4、C3H6 | B. | C2H4、C4H8 | C. | C3H4、C4H8 | D. | C3H4、C3H6 |
 在如图均用石墨作电极的电解池中,甲池中为500mL含某一溶质的蓝色溶液,乙池中为500mL稀硫酸,闭合K1,断开K2进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,立即停止电解,取出A电极,洗涤、干燥、称量,电极质量增重1.6g.请回答下列问题:
在如图均用石墨作电极的电解池中,甲池中为500mL含某一溶质的蓝色溶液,乙池中为500mL稀硫酸,闭合K1,断开K2进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,立即停止电解,取出A电极,洗涤、干燥、称量,电极质量增重1.6g.请回答下列问题: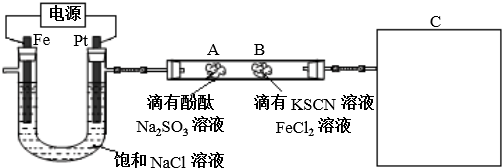
 他猜想:SCN-可能被氯水氧化,导致溶液变黄.
他猜想:SCN-可能被氯水氧化,导致溶液变黄.
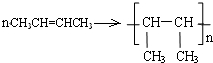 .
.