题目内容
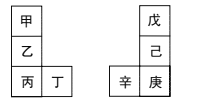
【题目】甲~辛等元素在周期表中的相对位置如图所示。甲与戊的原子序数相差3,戊是空气中含量最多的元素,丁与辛是同周期元素。下列说法正确的是( )
A.丙不能与水发生反应
B.己和氯气反应的产物只有一种
C.丙与庚的原子核外电子数相差13
D.乙形成的氧化膜疏松,不能保护内层金属
【答案】C
【解析】
戊是空气中含量最多的元素,则戊是N元素,甲与戊的原子序数相差3,则甲是Be,可推知乙是Mg,丙是Ca,丁是Sc元素,戊是N,己是P,庚是As,辛是Ge。
A.丙是Ca,Ca是活泼的金属,能够与水反应产生Ca(OH)2和H2,A错误;
B.己是P,P与Cl2反应产生PCl3、PCl5,产物不只有一种,B错误;
C.丙是Ca,原子序数是20,庚是As,原子序数是33,二者的原子序数差为33-20=13,C正确;
D.乙是Mg,乙形成的氧化膜MgO非常致密,能对内层的金属起保护作用,D错误;
故合理选项是C。

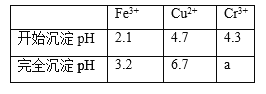
【题目】某温度下,0.200 molL-1的HA溶液与0.200 molL-1的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如下表,下列说法正确的是
微粒 | X | Y | Na+ | A- |
浓度/(mol·L-1) | 8.00 | 2.50 | 0.100 | 9.92 |
A. 0.1mol·L-1HA溶液的pH=1 B. 该温度下Kw=1.0![]() 10-14
10-14
C. 微粒X表示OH-,Y表示H+ D. 混合溶液中:n(A-)+n(X)=n(Na+)
【题目】某实验兴趣小组按下图装置实验后,所记录内容合理的是( )
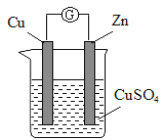
实验 记录 | ① Cu为正极,Zn为负极; ② Zn质量减少,Cu质量增加; ③ SO ④ 电子流方向是:由Zn经导线流入Cu片; ⑤ Zn电极发生还原反应; ⑥ 正极反应式:Cu2+ + 2e- = Cu |
A.②③④ B.①②④⑥ C.①②④⑤ D.②③⑤⑥