题目内容
【题目】(1)在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-。两步反应的能量变化示意图如下:
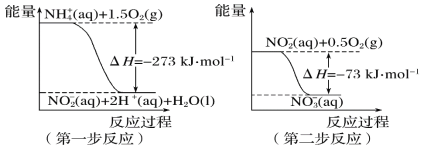
①第一步反应是________(填“放热”或“吸热”)反应,判断依据是______________。
②1molNH4+(aq)全部氧化成NO3- (aq)的热化学方程式是____________________。
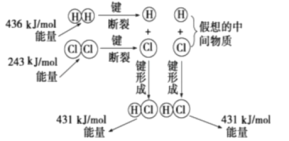
(2)如图所示是101kPa时氢气在氯气中燃烧生成氯化氢气体的能量变化,此反应的热化学方程式为_____________。
【答案】放热 ΔH<0或反应物的总能量大于生成物的总能量 NH4+(aq)+2O2(g)=NO3-(aq)+2H+(aq)+H2O(l) ΔH= -346 KJ/mol ![]()
【解析】
(1)①根据图像,第一步反应ΔH小于0,也可以根据应物的总能量大于生成物的总能量判断该反应为放热反应,故答案为:放热;ΔH<0或反应物的总能量大于生成物的总能量;
②第一步反应的热化学方程式为:![]() ,第二步反应的热化学方程式为:
,第二步反应的热化学方程式为:![]() ,两步反应相加,即可得到目标方程式:
,两步反应相加,即可得到目标方程式:![]() ,故答案为:
,故答案为:![]() ;
;
(2)反应![]() ,焓变△H=反应物键能总和-生成物键能总和
,焓变△H=反应物键能总和-生成物键能总和![]() ,故该反应的热化学方程式为:
,故该反应的热化学方程式为:![]() ,故答案为:
,故答案为:![]() 。
。

练习册系列答案
相关题目