��Ŀ����
�������ƾ���[CaO2��8H2O]���ȶ����ʰ�ɫ������ˮ��������������Һ���㷺Ӧ���ڻ���ɱ��������������
��������ƾ�����Ʊ�
��ҵ������CaO2��8H2O����Ҫ�������£�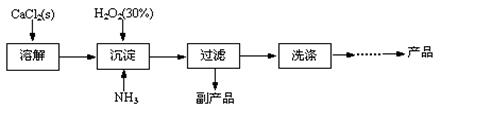
��1��������������ȡCaO2��8H2O�Ļ�ѧ����ʽ�� ��
��2������ʱ���ñ�ˮ�����¶���10�����º�ͨ�������NH3�������ԭ��ֱ���
�� ���� ��
��������ƾ��庬���IJⶨ
ȷ��ȡ0.3000g��Ʒ����ƿ�У�����30 mL����ˮ��10 mL 2.000 mol��L��1 H2SO4����0.0200mol��L��1 KMnO4����Һ�ζ����յ㡣�ظ������������Ρ�H2O2��KMnO4��Ӧ�����ӷ���ʽΪ2MnO4����5 H2O2��6H+��2Mn2+��5O2����8H2O
��3���ζ��յ�۲쵽������Ϊ ��
��4�����ݱ�1���ݼ����Ʒ��CaO2��8H2O������������д��������̣���
| �ζ����� | ��Ʒ������/g | KMnO4��Һ�����/mL | |
| �ζ�ǰ�̶�/mL | �ζ���̶�/mL | ||
| 1 | 0.3000 | 1.02 | 24.04 |
| 2 | 0.3000 | 2.00 | 25.03 |
| 3 | 0.3000 | 0.20 | 23.24 |
��1. KMnO4����Һ�ζ�����
��1��CaCl2+H2O2+2NH3+8H2O=CaO2��8H2O��+2NH4Cl����2�����¶ȵͿɼ��ٹ�������ķֽ⣬��߹�������������ʣ����ֹ��������ķֽ⣩����ͨ�������NH3ʹ��Һ�ʼ��ԣ�����CaO2��8H2O���ܽ⣨����߲�Ʒ�IJ��ʣ�����3�����������һ��KMnO4����Һ������ɫ��dz��ɫ���Ұ�����ڲ���ɫ����4��82.91% 5 CaO2��8H2O �� 5 H2O �� 2 KMnO4
n(CaO2��8H2O)=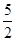 n(KMnO4)=
n(KMnO4)= 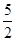 ��0.0200mol/L��23.03mL��10-3L/mL=1.1151��10-3mol������CaO2��8H2O������������
��0.0200mol/L��23.03mL��10-3L/mL=1.1151��10-3mol������CaO2��8H2O������������ =82.91%
=82.91%
����

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д���SiO2��3C SiC��2CO����Ӧ�У��������ͻ�ԭ����������Ϊ( )
SiC��2CO����Ӧ�У��������ͻ�ԭ����������Ϊ( )
| A��36��30 | B��60��36 | C��2��1 | D��1��2 |
����I2O5������CO��Ⱦ�����ⶨCO����ӦΪ��5CO��g����I2O5��s�� 5CO2��g����I2��s������H 1
5CO2��g����I2��s������H 1
��1����֪��2CO��g����O2��g�� 2CO2��g������H 2
2CO2��g������H 2
2I2��s����5O2��g�� 2I2O5��s������H 3
2I2O5��s������H 3
��H 1�� ���ú���H 2�ͦ�H 3�Ĵ���ʽ��ʾ����
��2����ͬ�¶��£���װ������I2O5�����2 L�����ܱ�������ͨ��2molCO�����CO2����������գ�CO2����ʱ��t�仯������ͼ����ش�
�ٴӷ�Ӧ��ʼ��a��ʱ�ķ�Ӧ����Ϊv(CO)�� ��b��ʱ��ѧƽ�ⳣ��Kb�� ��
��d��ʱ���¶Ȳ��䣬�����������ѹ����ԭ����һ�룬����ͼ�в��仭��CO2��������ı仯���ߡ�
������˵����ȷ���� ��������ĸ��ţ�
| A�������������ܶȲ��䣬������Ӧ�ﵽƽ��״̬ |
| B�������¶��£�c��ʱ��ϵ�л�������ƽ����Է���������� |
| C������I2O5��Ͷ�������������CO��ת���� |
| D��b���d��Ļ�ѧƽ�ⳣ����Kb��Kd |
 ��Fe(NO3)3��NO����2H2O
��Fe(NO3)3��NO����2H2O
