题目内容
6.若NA表示阿伏加德罗常数的值,下列说法正确的是( )| A. | 1mol OH-含有的电子数为9NA | |
| B. | 常温常压下,NO2和N2O4的混合物23g中含有NA个氧原子 | |
| C. | 标准状况下,2.8gN2和2.24L CO所含电子数均为1.4NA | |
| D. | 标准状况下,22.4 L 乙醇中含有NA个乙醇分子 |
分析 A、氢氧根中含10mol电子;
B、NO2和N2O4的最简式均为NO2;
C、标况下2.24LCO的物质的量为0.1mol;
D、标况下乙醇为液态.
解答 解:A、氢氧根中含10mol电子,故1mol氢氧根中含10mol电子即10NA个,故A错误;
B、NO2和N2O4的最简式均为NO2,故23g混合物中含有的NO2的物质的量为n=$\frac{23g}{46g/mol}$=0.5mol,故含1mol氧原子即NA个,故B正确;
C、2.8g氮气的物质的量为0.1mol,标况下2.24LCO的物质的量也为0.1mol,而氮气和CO中均含14个电子,故0.1mol氮气和CO中含有的电子均为1.4mol,个数为1.4NA个,故C错误;
D、标况下乙醇为液态,故不能根据气体摩尔体积来计算其物质的量,故D错误.
故选BC.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
1.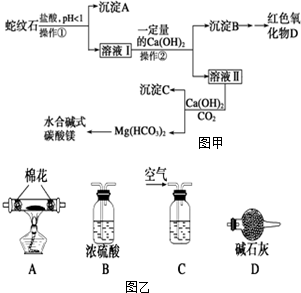 蛇纹石可以看作由MgO、Fe2O3、Al2O3、SiO2组成.实验室以蛇纹石为原料制取水合碱式碳酸镁,已知:
蛇纹石可以看作由MgO、Fe2O3、Al2O3、SiO2组成.实验室以蛇纹石为原料制取水合碱式碳酸镁,已知:
实验步骤如图甲,请回答下列问题:
(1)实验室完成操作①所用到的玻璃仪器有玻璃棒、漏斗、烧杯.
(2)检验溶液Ⅱ中是否含有Fe3+的操作与结论是取少量溶液Ⅱ于试管中,加入KSCN溶液,若无明显现象,说明溶液Ⅱ不含Fe3+;若溶液变红色,说明溶液Ⅱ含有Fe3+
(3)从沉淀混合物B中制取D,应加入一种试剂进行分离,其反应的离子方程式为OH-+Al(OH)3═AlO2-+2H2O,再进行过滤、洗涤、加热(依次填写实验操作名称).
(4)操作②中应控制溶液pH的合理范围是C(填序号).
A.小于1.5 B.1.5~3.3 C.7~8 D.大于9.4
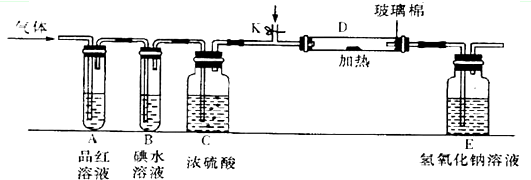
(5)为探究所得的水合碱式碳酸镁[xMgCO3•yMg(OH)2•zH2O]的组成,取样7.28g于装置A的玻璃管中,请按由左-→右顺序将如图乙装置连接好(填序号,装置可重复使用)C-→B-→A-→B-→D-→B(或D),装置C应盛的试剂是氢氧化钠溶液.充分反应后,如果实验测得硬质玻璃管中剩余固体3.2g,共放出2.64g CO2气体,则x:y:z=3:1:3.
 蛇纹石可以看作由MgO、Fe2O3、Al2O3、SiO2组成.实验室以蛇纹石为原料制取水合碱式碳酸镁,已知:
蛇纹石可以看作由MgO、Fe2O3、Al2O3、SiO2组成.实验室以蛇纹石为原料制取水合碱式碳酸镁,已知:| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 9.4 |
(1)实验室完成操作①所用到的玻璃仪器有玻璃棒、漏斗、烧杯.
(2)检验溶液Ⅱ中是否含有Fe3+的操作与结论是取少量溶液Ⅱ于试管中,加入KSCN溶液,若无明显现象,说明溶液Ⅱ不含Fe3+;若溶液变红色,说明溶液Ⅱ含有Fe3+
(3)从沉淀混合物B中制取D,应加入一种试剂进行分离,其反应的离子方程式为OH-+Al(OH)3═AlO2-+2H2O,再进行过滤、洗涤、加热(依次填写实验操作名称).
(4)操作②中应控制溶液pH的合理范围是C(填序号).
A.小于1.5 B.1.5~3.3 C.7~8 D.大于9.4
(5)为探究所得的水合碱式碳酸镁[xMgCO3•yMg(OH)2•zH2O]的组成,取样7.28g于装置A的玻璃管中,请按由左-→右顺序将如图乙装置连接好(填序号,装置可重复使用)C-→B-→A-→B-→D-→B(或D),装置C应盛的试剂是氢氧化钠溶液.充分反应后,如果实验测得硬质玻璃管中剩余固体3.2g,共放出2.64g CO2气体,则x:y:z=3:1:3.
11.已知10HNO3(稀)+4Zn=4Zn(NO3)2+a+5H2O,若a为氮的氧化物,则a为( )
| A. | NO | B. | NO2 | C. | N2O | D. | N2O3 |
18.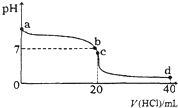 室温下,将0.1mol•L-1盐酸滴入20mL 0.1mol•L-1氨水中,溶液pH随加入盐酸体积的变化曲线如图所示.下列有关说法不正确的是( )
室温下,将0.1mol•L-1盐酸滴入20mL 0.1mol•L-1氨水中,溶液pH随加入盐酸体积的变化曲线如图所示.下列有关说法不正确的是( )
 室温下,将0.1mol•L-1盐酸滴入20mL 0.1mol•L-1氨水中,溶液pH随加入盐酸体积的变化曲线如图所示.下列有关说法不正确的是( )
室温下,将0.1mol•L-1盐酸滴入20mL 0.1mol•L-1氨水中,溶液pH随加入盐酸体积的变化曲线如图所示.下列有关说法不正确的是( )| A. | a点的pH>7,但Kw仍为1.0×10-14 | |
| B. | b点所示溶液中C(Cl-)=C(NH4+) | |
| C. | C点溶液pH<7,其原因是NH4++H2O?NH3•H2O+H+ | |
| D. | d点所示溶液中离子浓度由大到小的排序是:c(Cl-)>C(NH4+)>C(H+)>C(OH-) |
16.下列各项操作或现象能达到预期实验目的是( )
| 选项 | 操作或现象 | 实验目的 |
| A | 将铁钉放入试管中,用盐酸浸没 | 验证铁的吸氧腐蚀 |
| B | 向NaBr溶液中滴入少量氯水和苯,振荡、静置,溶液上层呈橙红色 | 证明Br-还原性强于Cl- |
| C | 将氯化亚铁固体溶于适量蒸馏水中 | 配制FeCl2溶液 |
| D | 将混有氯化氢杂质的氯气通过装有饱和NaHCO3溶液的洗气瓶 | 除去氯气中的HCl气体 |
| A. | A | B. | B | C. | C | D. | D |
17.如图实验操作正确的是( )
| A. | 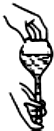 检验容量瓶是否漏水 | B. | 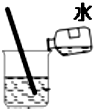 稀释浓硫酸 | ||
| C. | 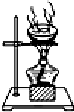 蒸发 | D. | 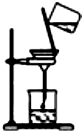 过滤 |
 ;
;
 2SO3.
2SO3.