题目内容
10.A、B、C、D是初中化学常见的物质,这四种物质中均含有同一种元素.其中A为无色气体单质,B、C为氧化物,且B为有毒气体,D是大理石的主要成分.它们之间的部分转化关系如图所示(图中反应条件及部分反应物、生成物已省略).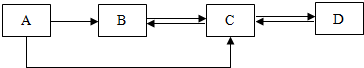
回答下列问题:
(1)写出下列物质的化学式:AO2;DCaCO3.
(2)写出由物质C转化为物质B的化学方程式CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO.从能量角度看,此反应属于吸热(填“放热”或“吸热”)反应
(3)若A为固体单质,写出A与一种黑色粉末反应转化为C的化学反应方程式C+2CuO$\frac{\underline{\;\;△\;\;}}{\;}$2Cu+CO2.
分析 根据A、B、C、D是初中化学常见的物质,D是大理石的主要成分,所以D是CaCO3,B、C为氧化物,由转化关系可知C为CO2,B为有毒气体,所以B是CO,A为无色气体单质,会转化成一氧化碳和二氧化碳,所以A是O2,以此解答该题.
解答 解:A、B、C、D是初中化学常见的物质,D是大理石的主要成分,所以D是CaCO3,B、C为氧化物,由转化关系可知C为CO2,B为有毒气体,所以B是CO,A为无色气体单质,会转化成一氧化碳和二氧化碳,所以A是O2,
(1)由以上分析可知A是O2,D是CaCO3,故答案为:O2;CaCO3;
(2)物质C转化为物质B的反应是二氧化碳和碳高温生成一氧化碳,化学方程式为:CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO,为吸热反应,故答案为:CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;吸热;
(3)C可与CuO反应生成CO2,反应的方程式为C+2CuO$\frac{\underline{\;\;△\;\;}}{\;}$2Cu+CO2,故答案为:C+2CuO$\frac{\underline{\;\;△\;\;}}{\;}$2Cu+CO2.
点评 本题考查无机物的推断,为高频考点,侧重于学生的分析能力的考查,涉及元素化合物知识的综合理解和运用的考查,注意相关基础知识的积累,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.为测某镁铝合金样品中铝的含量,某实验小组进行了下列实验:取一定量合金,加入100mL0.3mol•L-1稀硫酸,合金完全溶解,产生的气体在标准状况下体积为560mL;再不断滴加0.2mol•L-1NaOH溶液至沉淀质量恰好在此时不再变化,用去350mL NaOH溶液.则所取样品中铝的物质的量为( )
| A. | 0.005mol | B. | 0.01mol | C. | 0.025mol | D. | 0.03mol |
5.将5.32g纯Fe溶于足量稀H2SO4中,在加热条件下用2.53gKNO3去氧化溶液中的Fe2+,充分反应后余下的Fe2+还原0.009mol Cl2才能完全氧化,则KNO3的还原产物中N的化合价是( )
| A. | -3 | B. | +4 | C. | +3 | D. | +2 |
9.某无色溶液能与铝作用放出H2,则下列离子组合中可能的是( )
| A. | H+、Cl-、Cu2+、Ba2+ | B. | OH-、NO${\;}_{3}^{-}$、Ba2+、Cl- | ||
| C. | H+、CO${\;}_{3}^{2-}$、Mg2+、Ba2+ | D. | OH-、NO${\;}_{3}^{-}$、CO${\;}_{3}^{2-}$、Mg2+ |
6.若NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1mol OH-含有的电子数为9NA | |
| B. | 常温常压下,NO2和N2O4的混合物23g中含有NA个氧原子 | |
| C. | 标准状况下,2.8gN2和2.24L CO所含电子数均为1.4NA | |
| D. | 标准状况下,22.4 L 乙醇中含有NA个乙醇分子 |
8.证明NaHSO3溶液中HSO3-的电离程度大于水解程度,可采用的实验方法是( )
| A. | 加入盐酸 | B. | 加入Ba(OH)2溶液 | C. | 测定溶液的pH值 | D. | 加入品红溶液 |
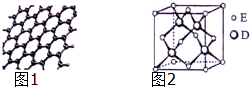 原子序数依次增大的五种元素A、B、C、D、E位于周期表的前四周期.A基态原子的2p轨道上有2个未成对电子;C的最外层电子数是次外层电子数的3倍,C与D同主族相邻;E位于周期表的ds区,最外层只有一对成对电子.请回答下列问题:
原子序数依次增大的五种元素A、B、C、D、E位于周期表的前四周期.A基态原子的2p轨道上有2个未成对电子;C的最外层电子数是次外层电子数的3倍,C与D同主族相邻;E位于周期表的ds区,最外层只有一对成对电子.请回答下列问题: