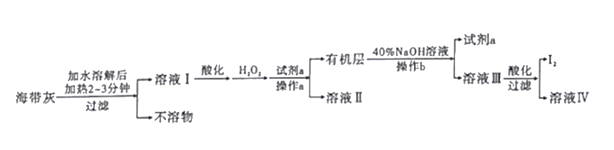
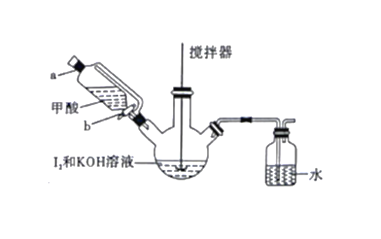
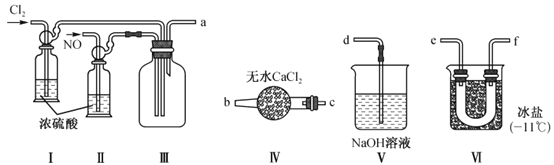
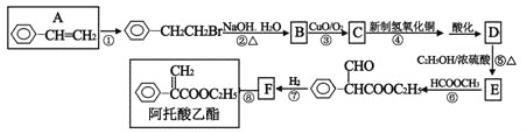
题目内容
【题目】某研究性学习小组设计了一组实验验证元素周期律。
Ⅰ.为了用实验的方法验证镁和铝的金属性强弱,学生甲和学生乙分别设计了两种不同的方法:
方案一:学生甲用水作试剂,比较镁和铝与水反应的情况
方案二:学生乙用稀盐酸作试剂,比较镁和铝与稀盐酸反应的情况
(1)以上两实验方案实验现象较为明显的是方案___________________________。
(2)学生乙在实验中取了一段黑色的镁带,投入稀盐酸中,现象不十分明显,请分析原因____。
(3)学生内另辟蹊径,不用镁、铝的单质,而用镁、铝的可溶盐及一些其它化学试剂,进行实验也得出正确的结论,简述学生丙用的是什么方法?_____________________________。
Ⅱ.学生丁设计了下图装置以验证硫、碳、硅元素的非金属性强弱。已知B是一种正盐,是工业生成玻璃的主要原料之一。
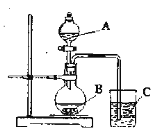
(1)写出所选用物质的化学式:A:__________________,B:____________________。
(2)写出烧杯中发生反应的离子方程式:_________________________________。
【答案】方案二 未除去镁表面的氧化膜 取镁、铝的可溶盐逐滴加氢氧化钠溶液均产生氢氧化物沉淀,过量碱液可使生成的Al(OH)3溶解,而Mg(OH)2则不溶 H2SO4 Na2CO3 CO2+SiO32-+H2O![]() H2SiO3↓+CO32-或:2CO2+SiO32-+2H2O
H2SiO3↓+CO32-或:2CO2+SiO32-+2H2O![]() H2SiO3↓+2HCO3-
H2SiO3↓+2HCO3-
【解析】
Ⅰ(1)从实验操作是否简单,实验现象是否明显角度分析;
(2)镁条表面有氧化镁,反应现象不明显;
(3)根据氢氧化镁、氢氧化铝是否溶于强碱设计;
Ⅱ.元素非金属性越强,其最高价氧化物水化物酸性越强,利用强酸制备弱酸进行设计实验,A是硫酸;B是碳酸钠,C为硅酸钠;
Ⅰ(1)常温下镁和铝几乎不和水发生反应,而和酸反应较明显,所以方案二更好;
答案:方案二
(2)根据生成气体的剧烈程度判断金属性强弱,但镁条表面有氧化镁,未除去镁表面的氧化膜,所以反应现象不明显;
答案:未除去镁表面的氧化膜
(3)根据氢氧化镁、氢氧化铝是否溶于强碱设计,具体方法:取镁、铝的可溶盐逐滴加氢氧化钠溶液均产生氢氧化物沉淀,过量碱液可使生成的Al(OH)3溶解,而Mg(OH)2则不溶;
答案:取镁、铝的可溶盐逐滴加氢氧化钠溶液均产生氢氧化物沉淀,过量碱液可使生成的Al(OH)3溶解,而Mg(OH)2则不溶。
Ⅱ实验设计中涉及的反应①H2SO4+Na2CO3=Na2SO4+H2O+CO2↑,证明硫酸酸性强于碳酸,因此硫的非金属性强于碳;②CO2+Na2SiO3+H2O![]() H2SiO3↓+Na2CO3或2CO2+Na2SiO3+2H2O
H2SiO3↓+Na2CO3或2CO2+Na2SiO3+2H2O![]() H2SiO3↓+2NaHCO3,证明碳酸酸性强于硅酸,因此碳的非金属性强于硅。
H2SiO3↓+2NaHCO3,证明碳酸酸性强于硅酸,因此碳的非金属性强于硅。
(1)由以上分析可知A:H2SO4,B:Na2CO3;
答案:H2SO4, Na2CO3
(2)烧杯中发生反应的离子方程式:CO2+SiO32-+H2O![]() H2SiO3↓+CO32-或:2CO2+SiO32-+2H2O
H2SiO3↓+CO32-或:2CO2+SiO32-+2H2O![]() H2SiO3↓+2HCO3-;
H2SiO3↓+2HCO3-;
答案:CO2+SiO32-+H2O![]() H2SiO3↓+CO32-或:2CO2+SiO32-+2H2O
H2SiO3↓+CO32-或:2CO2+SiO32-+2H2O![]() H2SiO3↓+2HCO3-;
H2SiO3↓+2HCO3-;

【题目】下列关于卤素的说法正确的是
A. “加碘食盐”中的“碘”是指I2 B. 液溴有强挥发性,保存时应加少量水液封
C. F2可以从NaCl水溶液中置换出Cl2 D. 卤化氢都易溶于水,其水溶液都是强酸
【题目】I.请根据信息填空:
(1)FeCl3溶液常用于腐蚀印刷电路铜板,发生反应2FeCl3 +Cu ===2FeCl2 +CuCl2,若将此反应设计成原电池,则负极所用的电极材料为__________________;当线路中转移0.2mol电子时,则被腐蚀的铜的质量为__________________。
(2)如图所示,把试管放入盛有25℃的饱和澄清石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5 mL盐酸于试管中,可观察到溶液变浑浊,试回答下列问题:
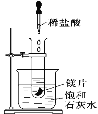
①产生上述现象的原因是___________________________;
②写出有关反应的离子方程式___________________。
③由实验推知,MgCl2溶液和H2的总能量__________(填“大于”、“小于”或“等于”)镁片和盐酸的总能量。
Ⅱ.在1×105 Pa和298 K时,将1 mol气态AB分子分离成气态A原子和B原子所需要的能量称为键能(kJ·mol-1)。下面是一些共价键的键能:(已知氨分子中有三个等价的氮氢共价键)
共价键 | H2分子 | N2分子 | NH3分子 |
键能(kJ·mol-1) | 436 | 945 | 391 |
(1)根据上表中的数据判断工业合成氨的反应是______(填“吸热”或“放热”)反应;
(2)在298 K时,取1 mol N2和3 mol H2放入一密闭容器中,在催化剂存在下进行反应,理论上生成2molNH3时放出或吸收的热量为Q,则Q为________。